下列说法正确的是
| A.增大反应物浓度,可增大活化分子的百分数,从而使有效碰撞次数增大; |
| B.有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大; |
| C.升高温度能使化学反应速率增大,主要原因是增加了反应物分子中活化分子的百分数; |
| D.催化剂不影响反应活化能但能增大单位体积内活化分子百分数,从而增大反应速率。 |
某金属单质跟一定浓度的硝酸反应,假定只产生单一的还原产物,当参加反应的单质与被还原硝酸的物质的量之比为2∶1时,还原产物是
| A.NO2 | B.NO | C.N2O | D.N2 |
将相同质量的铜片分别和过量浓硝酸、稀硝酸反应,下列叙述正确的是
| A.反应速率,两者相同 |
| B.消耗硝酸的物质的量:前者多,后者少 |
| C.反应生成气体的颜色:前者浅,后者深 |
| D.反应中转移的电子总数:前者多,后者少 |
在一定温度和压强下,将装有N2和NO2混合气体的试管倒立于水槽中,最后试管内气体的体积缩小为原体积的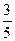 ,则混合气体中N2与NO2的体积比是
,则混合气体中N2与NO2的体积比是
| A.2:3 | B.3:2 | C.3:5 | D.5:3 |
X、Y、Z三种气体,取X和Y按1:1的物质的量之比混合,放入密闭容器中发生如下反应:X+2Y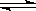 2Z ,达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3:2,则Y的转化率最接近于
2Z ,达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3:2,则Y的转化率最接近于
| A.33% | B.40% | C.50% | D.67% |
一种新型燃料电池,以镍板为电极插入KOH溶液中,分别向两极通乙烷和氧气,电极反应式为:C2H6+18OH--14e-=2CO32-+12H2O;7H2O+7/2O2+14e-=14OH-。有关此电池的推断正确的是
| A.通氧气的电极为负极 |
| B.参加反应的O2与C2H6的物质的量之比为7∶2 |
| C.电池工作一段时间后,KOH的物质的量浓度不变 |
| D.电池工作时,溶液中OH-离子向正极移动 |