将N2、H2的混合气体分别充入甲、乙、丙三个容器中,进行合成氨反应 N2+3H2  2NH3,经过相同的一段时间后,测得反应速率分别为:甲:v(H2)=3 mol·L-1·min-1;乙:v(N2)=2 mol·L-1·min-1;丙:v(NH3)= 1 mol·L-1·min-1。则三个容器中合成氨的反应速率
2NH3,经过相同的一段时间后,测得反应速率分别为:甲:v(H2)=3 mol·L-1·min-1;乙:v(N2)=2 mol·L-1·min-1;丙:v(NH3)= 1 mol·L-1·min-1。则三个容器中合成氨的反应速率
| A.v(乙)>v(甲)>v(丙) | B.v(乙)>v(丙)>v(甲) |
| C.v(丙)>v(甲)>v(乙) | D.v(甲)>v(乙)>v(丙) |
下列化学反应属于吸热反应的是
| A.碘的升华 | B.生石灰溶于水 |
| C.镁与稀盐酸反应 | D.熟石灰与NH4Cl晶体混合制氨 |
“美丽中国”是十八大提出的重大课题,她突出了生态文明,重点是社会发展与自然环境之间的和谐,下列行为中不符合这一主题的是
| A.用已脱硫的煤作燃料 |
| B.开发太阳能、风能和氢能等能源代替化石燃料,有利于节约资源、保护环境 |
| C.采用“绿色化学”工艺,使原料尽可能转化为所需要的物质 |
| D.开发利用可燃冰是缓解能源紧缺的唯一途径 |
已知断开1 mol H2中的化学键需要吸收436kJ的能量,断开1 mol Cl2中的化学键需要吸收243kJ的能量,而形成1mol HCl分子中的化学要释放431kJ的能量,则1mol氢气与1mol氯气反应时能量变化为
| A.吸收183kJ | B.吸收366kJ | C.放出183kJ | D.放出366kJ |
已知X、Y、Z、W、R是原子序数依次增大的短周期主族元素,X是原子半径最小的元素,Y的最高正价与最低负价的代数和为0,Z的二价阳离子与氖原子具有相同的核外电子排布,W原子最外层电子数是最内层电子数的3倍。下列说法正确的是
| A.R的原子半径比Z的大 |
| B.R的氢化物的热稳定性比W的强 |
| C.X与Y形成的化合物只有一种 |
| D.Y的最高价氧化物的水化物的酸性比W的 |
下图是电解CuCl2溶液的装置,其中c、d为石墨电极,则下列有关的判断正确的是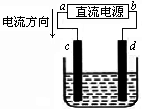
| A.a为负极、b为正极 |
| B.a为阳极、b为阴极 |
| C.电解过程中,d电极质量增加 |
| D.电解过程中,氯离子浓度不变 |