工业制硫酸中的一步重要反应是SO2在400-500℃下的催化氧化:2SO2+O2=2SO3,这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法中错误的是
| A.使用催化剂是为了加快反应速率,提高生产效率 |
| B.在上述条件下,SO2不可能100%转化为SO3 |
| C.为了提高SO2的转化率,应适当提高O2的浓度 |
| D.达到平衡时,SO2的浓度与SO3的浓度相等 |
下列有关比较中,大小顺序排列错误的是()
| A.分散系中分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液 |
| B.物质的熔点:石英>食盐>冰>汞 |
| C.晶体的晶格能CaO>NaCl>CsCl |
| D.热稳定性:PH3>H2S>HBr>NH3 |
图表资料可以为我们提供很多信息,下列关于图表提供的资料或应用的说法中,不正确的是() NvQ"xKN
| A.利用元素周期表可以预测新元素的原子结构和性质MRI7 ? |
| B.根据酸、碱、盐的溶解性表,可判断酸、碱、盐的溶解度 hk]7>}eYn? |
| C.根据电负性表,可判定2种元素形成的化学键是离子键还是共价键 d:="}5JGIQ" |
| D.核磁共振氢谱可以用来测定分子中H原子种类和个数比 |
二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂;其分子结构如右下图所示。S2Cl2遇水易水解,并产生能使品红褪色的气体。下列说法中错误的是()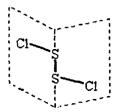

A.S2Cl2固体为分子晶体 |
||
B.S2Cl2为含有极性键和非极性键的非极性分子 |
C.S2Br2与S2Cl2结构相似,熔沸点:S2Br2>S2Cl2 |
D.S2Cl2中硫元素化合价为+1,与H2O反应可能属于氧化还原反应,方程式如下: 2S2Cl2+2H2O=SO2↑+3S↓+4HCl 2S2Cl2+2H2O=SO2↑+3S↓+4HCl |
由硫酸钾、硫酸铝和硫酸组成的混合溶液,其pH=1,c(Al3+)=0.4mol·L-1,c(SO42-)=0.8mol·L-1,则c(K+)为( )
| A.0.15 mol·L-1 | B.0.2 mol·L-1 | C.0.3 mol·L-1 | D.0.4 mol·L-1 |
对H2O的电离平衡不产生影响的粒子是()
A.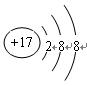 |
B.M3+离子核外电子排布式:[Ar]3d5 |
C.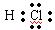 |
D.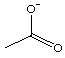 |