用铜片、银片、Cu (NO3)2溶液、AgNO3溶液、导线和盐桥(装有琼脂-KNO3的U型管)构成一个原电池。以下有关该原电池的叙述正确的是( )
①在外电路中,电流由铜电极流向银电极 ②正极反应为:Ag++e-=Ag
③实验过程中取出盐桥,原电池仍继续工作
④将铜片浸入AgNO3溶液中发生的化学反应与该原电池反应相同
| A.①② | B.②③ | C.②④ | D.③④ |
硝酸被称为“国防工业之母”是因为它是制取炸药的重要原料。下列实验事实与硝酸性质不相对应的一组是 ( )
| A.浓硝酸使紫色石蕊试液先变红后褪色——酸性和强氧化性 |
| B.不能用稀硝酸与锌反应制氢气——强氧化性 |
| C.要用棕色瓶盛装浓硝酸——不稳定性 |
| D.稀硝酸能使滴有酚酞的氢氧化钠溶液红色褪去——强氧化性 |
短周期金属元素A~E在元素周期表中的相对位置如表所示,下面判断正确的是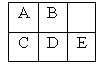
| A.原子半径:C<D<E |
| B.金属性:A>C |
| C.氢氧化物的化学式及其碱性:COH>D(OH)2>E(OH)3 |
| D.最外层电子数:A>B |
A元素原子最外层电子数是次外层电子数的3倍,B元素原子次外层是最外层电子数的2倍,则关于A、B元素的判断正确的
A. A和B元素不一定都是短周期元素 B. A和B元素一定是同一主族元素
C.A和B元素一定都是非金属元素 D. A、B可以相互化合形成化合物BA2或B2A
下列说法正确的是
①元素原子的最外层电子数等于元素的最高化合价
②最外层一个电子的元素一定是金属元素,肯定在元素周期表的第IA族
③所有元素的原子最外层最多可容纳的电子数均为8
④第三周期元素随原子序数增大各非金属元素对应的氧化物的水化物酸性一定逐渐增强
⑤同主族元素随原子序数增大,其原子半径逐渐增大
| A.①②③④⑤ | B.①②③ | C.④⑤ | D.⑤ |
以下关于第IA族元素和第ⅦA族元素的有关叙述正确的是
| A.从上到下,第IA族元素单质的密度逐渐增大 |
| B.从上到下,第IA族元素单质的熔点逐渐降低 |
| C.从上到下,第ⅦA族元素其氢化物的稳定性逐渐增强 |
| D.从上到下,第ⅦA族元素其氢化物的沸点逐渐升高 |