某小组为研究电化学原理,设计如图2装置。下列叙述不正确的是
| A.a和b不连接时,铁片上会有金属铜析出 |
| B.a和b用导线连接时,铜片上发生的反应为:Cu2++2e-===Cu |
| C.无论a和b是否连接,铁片均会溶解,溶液均从蓝色逐渐变成浅绿色 |
| D.a和b分别连接直流电源正、负极,电压足够大时,Cu2+向铜电极移动 |
下列溶液中,有关离子一定能大量共存的是
| A.能使石蕊呈蓝色的溶液中: Na+、I-、Cl-、NO3- |
| B.能使甲基橙呈黄色的溶液中:K+、SO32-、SO42-、ClO- |
| C.能使pH试纸变红色的溶液中:Mg2+、Fe3+、NO3-、[Ag(NH3)2]+ |
D.无色溶液中:K+、Cl-、NO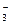 、SO 、SO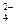 |
阿伏加德罗常数的值约为6.02×1023mol-1,下列叙述中不正确的是
①12.4g白磷晶体中含有的P-P键数约是0.6×6.02×1023
②电解精炼铜时转移了6.02×1023个电子,阳极溶解32 g铜
③7.8 g Na2S和Na2O2的混合物中含有的阴离子数大于0.1×6.02×1023
④2mol SO2和1 mol O2混合在V2O5存在的条件下于密闭容器中加热反应后,容器内物质分子数大于2×6.02×1023
⑤2.9g 2CaSO4·H2O含有的结晶水分子数为0.02×6.02×1023(2CaSO4·H2O式量为290)
⑥含0.2 mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数为0.1 NA
| A.①④⑥ | B.①③④⑤⑥ | C.②③⑤⑥ | D.③④⑤⑥ |
下列离子方程式中正确的是
| A.稀硫酸滴在铜片上:Cu + 2H+= Cu2++H2↑ |
| B.用小苏打治疗胃酸过多:HCO3-+ H+= H2O + CO2↑ |
| C.硝酸滴在石灰石上:CaCO3+ 2H+= Ca2++H2CO3 |
| D.醋酸钠和盐酸混和:CH3COONa + H+= CH3COOH + Na+ |
向饱和石灰水中不断通入二氧化碳,其溶液导电性的变化是
| A.由弱变强 | B.由强变弱 | C.由强变弱,再变强 | D.由弱变强,再变弱 |
用NA表示阿伏加德罗常数的值。下列叙述正确的是
| A.1mol·L-1NaCl溶液含有NA个Na+ |
| B.任意条件下,16g O3所含的原子数为NA |
| C.由CH4和C2H6组成的混合物中共有NA个分子,其中的氢原子数为5NA |
| D.标准状况下,22.4 L SO3所含的分子数为NA |