下列实验能达到预期目的的是
①淀粉加稀硫酸水解后,立即加入新制氢氧化铜溶液,可以检验产物是否含有葡萄糖
②可以用NaOH溶液除去溴苯中混有的少量溴
③为除去乙醇中含有的水,加入足量生石灰,再蒸馏
④用加热的方法提取NH4Cl固体中混有的少量碘
⑤用碘酒验证汽油中是否含有不饱和烃
| A.①④⑤ | B.②③⑤ | C.②③④⑤ | D.全部都可以 |
已知N2+3H2=2NH3 △H<0,硫化氢难电离。下列事实不能用勒夏特列原理解释的是:
| A.给硫化氢水溶液中加碱有利于S2-的生成 |
| B.加入催化剂有利于氨的氧化反应 |
| C.高压有利于合成氨反应 |
| D.500℃左右比室温更利于合成氨的反应 |
在一定温度下,反应A2(气)+ B2(气) 2AB(气)达到平衡的标志是:
2AB(气)达到平衡的标志是:
| A.单位时间生成的n mol的A2同时生成2n mol的AB |
| B.容器内的总压强不随时间变化 |
| C.单位时间生成2n mol的AB同时生成n mol的B2 |
D.单位时间生成 n mol的A2同时生成n mol的B2 n mol的A2同时生成n mol的B2 |
下列的平衡移动图中,其中能表示由于减少反应物浓度引起化学平衡移动的是: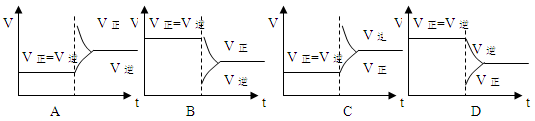
反应2X(g)+Y(g) 2Z(g)+热量,在不同温度(T1和T2
2Z(g)+热量,在不同温度(T1和T2 )及压强(p1和p2)下,产物Z的物质的量[n(Z)]与反应时间(t)的关系如图所示。则下述判断正确的是:
)及压强(p1和p2)下,产物Z的物质的量[n(Z)]与反应时间(t)的关系如图所示。则下述判断正确的是: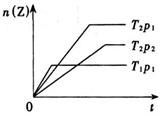
| A.T1<T2,p1<p2 | B.T1<T2,p1>p2 |
| C.T1>T2,p1>p2 | D.T1>T2,p1<p2 |
某温度下,浓度都是1 mol·L-1的两种气体X2和Y2,在密闭容器中反应生成气体Z,反应平衡时,测得物质的浓度分别为:c(X2)=0.4 mol·L-1,c(Y2)=0.8 mol·L-1,c(Z)=0.4 mol·L-1,则该反应的反应式可表示为:
A.X2+2Y2 2XY2 2XY2 |
B.2X2+Y2 X2Y X2Y |
C.3X2+Y2 2X3Y 2X3Y |
D.X2+3Y2 2XY3 2XY3 |