在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入的NaOH溶液体积的关系如图所示,由此确定,原溶液中含有的阳离子是( )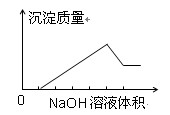
| A.Mg2+、Al3+、Fe2+ | B.H+、Mg2+、Al3+ |
| C.H+、Ba2+、Al3+ | D.只有Mg2+、Al3+ |
下列所采取的分离方法正确的是()
| A.由于碘在酒精中的溶解度大,所以可用酒精将碘水中的碘萃取出来 |
| B.水的沸点是100℃,酒精的沸点是78.5℃,所以可用直接加热蒸馏法使含水酒精变为无水酒精 |
| C.可用冷却热的饱和氯化钾和氯化钠混合溶液的方法得到纯净的氯化钠晶体 |
| D.由于胶体微粒的直径比离子大,所以碘化钾混入淀粉中可用渗析法分离 |
某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32−、SO42−、NO3−中的几种。①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如右图所示。
则下列说法正确的是
| A.溶液中的阳离子只有H+、Mg2+、Al3+ |
| B.溶液中n(NH4+)=0.2mol |
| C.溶液中一定不含CO32−,可能含有SO42−和NO3− |
| D.三种离子的物质的量之比:n(H+)∶n(Al3+)∶n(Mg2+) = 1∶1∶1 |

 某同学用沉淀法测定碳酸钠和氢氧化钠混合物中氢氧化钠的质量分数,有关叙述如下:
某同学用沉淀法测定碳酸钠和氢氧化钠混合物中氢氧化钠的质量分数,有关叙述如下:
①检验 是否完全沉淀的操作方法是,取上层清液装于试管,向试管滴加沉淀剂溶液
是否完全沉淀的操作方法是,取上层清液装于试管,向试管滴加沉淀剂溶液
②检验 是否完全沉淀的操作方法是向上层清液中继续滴加沉淀剂溶液
是否完全沉淀的操作方法是向上层清液中继续滴加沉淀剂溶液
③用氯化钡溶液代替氯化钙溶液作沉淀剂,优点是实验结果准确度较高
④用氯化钡溶液代替氯化钙溶液作沉淀剂,优点是碳酸钡能完全沉淀
其中正确的是()
| A.①③ | B.②③ | C.②④ | D.①④ |
 能正确表示下列反应离子方程式是
能正确表示下列反应离子方程式是
A.向次氯酸钙溶液通入过量C O2:Ca2++2ClO-+CO2+H2O =CaCO3↓+2HClO O2:Ca2++2ClO-+CO2+H2O =CaCO3↓+2HClO  |
B.向次氯酸钙溶液通入SO2:Ca2++2ClO-+SO2+H2O= CaSO3↓+2HClO  |
C.氢氧化钙溶液与碳酸氢镁溶液反应:HCO3-+Ca2++OH-=CaCO3↓+H2O  |
D.在氯化亚铁溶液中加入稀硝酸:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O  |
下列实验合理的是( )
 |
 |
 |
 |
| A、配制一定浓度硫酸 |
B、制备少量氨气 |
C、制备并收集少量NO2气体 |
D、制备少量氧气 |