已知某元素的一种原子可用符号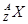 表示,则组成该元素一个原子的基本微粒总数是
表示,则组成该元素一个原子的基本微粒总数是
| A.Z | B.A | C.A+Z | D.A-Z |
下列溶液中的反应能用离子方程式H++OH-=H2O表示的是
| A.2NaOH+CO2=Na2CO3+H2O | B.NH3·H2O+HCl =NH4Cl+H2O |
| C.Mg(OH)2+2HCl =MgCl2+H2O | D.2KOH+H2SO4=K2SO4+2H2O |
在含有大量Na+、Cl-、OH-的溶液中还可能大量存在的离子是
| A.Fe2+ | B.Cu2+ | C.AlO2- | D.HCO3- |
下列操作中,溶液的颜色不发生变化的是
| A.碘水中滴加淀粉溶液 | B.溴化钠溶液中滴加氯水 |
| C.硫酸铁溶液中滴加硫氰化钾溶液 | D.盐酸中滴加酚酞试液 |
门捷列夫制作元素周期表时,许多元素尚未发现,他在铝的下面留了空位给“类铝”,并对“类铝”的性质进行了预测, “类铝”与后来发现的镓的性质一致,从而验证了元素周期表的正确性。下列有关镓的性质的描述中错误的是
| A.镓的金属性比铝弱 | B.镓的常见化合价为+3 |
| C.镓的原子半径比铝大 | D.镓的原子结构示意图为 |
Y元素最高正价与负价的绝对值之差为4,Y元素与M元素可形成离子化合物,该物质能溶于水并在水中电离出电子层结构相同的离子,该化合物是
| A.硫化钾 | B.硫化钠 | C.氯化钠 | D.氧化铝 |