应用元素周期律的有关知识,可以预测我们不知道的一些元素及其化合物的性质。下列预测中不正确的是( )
①Be的最高价氧化物的水化物可能具有两性
②H2Se是无色,有毒,比H2S稳定的气体
③At单质为有色固体,AgAt不溶于水也不溶于稀硝酸
④Li在氧气中剧烈燃烧,产物是Li2O2,其溶液是一种强碱
⑤SrSO4是难溶于水的白色固体
⑥B和Si的最高价氧化物的水化物均为H2XO3形式,且酸性很弱
| A.①②③④ | B.②④⑥ | C.①③⑤ | D.②④⑤ |
W、X、Y、Z是短周期元素,其部分性质如下表:
| W |
单质是淡黄色固体 |
| X |
在地壳中的含量居第二位 |
| Y |
原子最外层电子数是电子总数的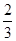 |
| Z |
第3周期原子半径最小的金属 |
下列说法正确的是
A.气态氢化物的热稳定性:X>W
B.非金属性:Y < W;离子半径:Z > W
C.W在空气中燃烧所得产物,可用于杀菌消毒
D.金属Z与少量NaOH溶液反应,生成两性氢氧化物
下列离子方程式与所述事实相符且正确的是
| A.向含有0.4 mol FeBr2的溶液中通入0.3 mol Cl2充分反应:4Fe2++2Br-+3Cl2=== 4Fe3++6Cl-+Br2 |
| B.磁性氧化铁溶于氢碘酸:Fe3O4+8H+=== 2Fe3++Fe2++4H2O |
| C.放置在空气中的淀粉碘化钾溶液一段时间后溶液呈蓝色:4H++4I-+O2===2I2+2H2O[来 |
| D.向硝酸铵溶液中滴加NaOH溶液:NH4++OH-=== NH3↑+ H2O |
下列现象及结论均正确的是
| 现象 |
结论 |
|
| A |
向Na2O2与水反应完的溶液中,滴加石蕊试液,溶液先变蓝后褪色 |
Na2O2与水反应后的溶液呈碱性,且有少量的Na2O2剩余,而氧化石蕊使其褪色 |
| B |
将盐酸与NaHCO3反应生成的CO2气体,直接通入Na2SiO3溶液中出现浑浊 |
说明碳的非金属性强于硅 |
| C |
Na2S溶液与Na2SO3溶液混合后出现浑浊 |
发生反应的离子方程式为: 2S2-+SO32-+3H2O === 3S↓+6OH- |
| D |
用饱和食盐水吸收氯气中混有的HCl气体,出现白色浑浊 |
白色浑浊为析出的氯化钠晶体 |
下列说法错误的是
| A.浓硫酸具有强氧化性,但SO2气体可以用浓硫酸干燥 |
| B.常温下实验室可以用稀硝酸与铁反应制取NO气体 |
| C.王水溶解金的过程为氧化还原反应,还原产物为NO2 |
| D.SiO2不仅能与氢氧化钠溶液反应,也能与氢氟酸反应 |
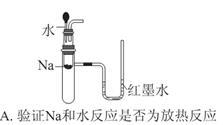
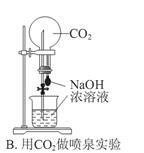
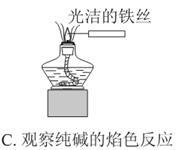
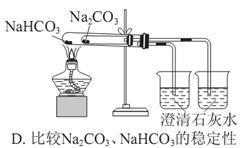
下列实验装置不能达到实验目的的是