下列结论错误的是( )
| A.氢化物的稳定性HF>HCl>H2S>PH3>SiH4 |
| B.微粒半径K+>Al3+>S2->Cl- |
| C.酸性:H2SO4>CH3COOH >H2CO3>HClO |
| D.金属性:K > Ca > Mg > Be |
物质分类的依据通常是根据它的组成和性质,下列物质分类中,只考虑组成的是
| A.硫酸钠是钠盐、硫酸盐、正盐 |
| B.二氧化硫是氧化物、酸酐、有漂白性物质 |
| C.氢氧化钠是一元碱、易溶性碱、强碱 |
| D.碳酸氢钠是钠盐、酸式盐、易分解的盐 |
下列说法不正确的是
| A.大气污染物主要来自化石燃料和工业生产过程产生的废气 |
| B.形成酸雨的主要物质是硫氧化物和氮氧化物(NOx) |
| C.绿色化学的核心就是在生产过程中减少污染 |
| D.水华、赤潮等水体污染是由于含氮、磷的大量污水任意排放造成的 |
下列离子方程式正确的是
| A.硫酸铜溶液与足量氢氧化钡溶液混合:Ba2++SO42-=BaSO4↓ |
| B.AgCl悬浊液中加入硫化钠饱和溶液:2AgCl + S2-=Ag2S +2Cl- |
C.硫化钠的水解反应:S2-+H3O+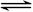 HS-+H2O HS-+H2O |
| D.用K37ClO3与浓盐酸制氯气:37ClO3-+6H++6Cl-=37Cl-+3Cl2↑+3H2O |
相同温度下,体积均为0.25L的两个恒容密闭容器中发生可逆反应:
X2(g) + 3Y2(g)  2XY3(g)△H=-92.6 kJ·mol-1
2XY3(g)△H=-92.6 kJ·mol-1
实验测得反应在起始、达到平衡时的有关数据如下表所示:
| 容器 编号 |
起始时各物质物质的量/mol |
达平衡时体系能量的变化 |
||
| X2 |
Y2 |
XY3 |
||
| ① |
1 |
3 |
0 |
放热 23.15 kJ |
| ② |
0.6 |
1.8 |
0.8 |
Q(Q>0) |
下列叙述不正确的是
A.容器①、②中反应的平衡常数相等
B.容器②中反应达到平衡时放出的热量Q为23.15kJ
C.达平衡时,两个容器中XY3的物质的量浓度均为2 mol·L-1
D.若容器①体积为0.20 L,则达平衡时放出的热量大于23.15 kJ
已知KHSO3溶液呈弱酸性。在0.1mol·L-1KHSO3溶液中,下列关系正确的是
| A.c(K+)+ c(H+) =c(HSO3-)+ c(OH-)+ c(SO32-) |
| B.c(HSO3-) + c(SO32-) = 0.1mol·L-1 |
| C.c(SO32-) < c(H2SO3) |
| D.c(K+) = c(H2SO3) + c(HSO3-) + c(SO32-) |