下列有关叙述正确的是( )
| A.元素性质呈周期性变化的根本原因是元素化合价呈周期性变化 |
| B.H2O和CO2分子中所有原子均满足最外层为8电子结构 |
| C.已知114号元素的一种核素的质量数为298,则该元素的相对原子质量为298 |
| D.18OD-中,电子数、质子数、中子数之比为 10∶9∶11 |
“垃圾是放错位置的资源”,应该分类回收。生活中废弃的铁锅、铝制易拉罐、铜导线
等可以归为一类予以回收,它们属于
| A.氧化物 | B.盐 | C.金属或合金 | D.碱 |
下列实验操作没有用到玻璃棒的是
| A.溶解 | B.萃取 | C.过滤 | D.蒸发结晶 |
金属钠着火时,可用来灭火的是
| A.CO2 | B.水 | C.煤油 | D.沙土 |
羰基硫(COS)可用作粮食熏蒸剂,可由CO 与H2S 在一定条件下反应制得。在恒容的密
闭容器中发生反应并达到平衡: ,数据如下表
,数据如下表
所示: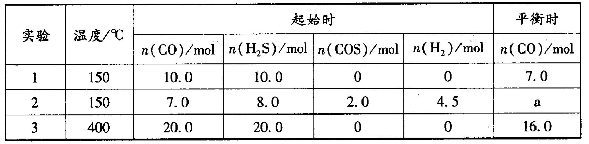
下列说法正确的是
| A.上述反应是吸热反应 |
| B.实验1 达平衡时,CO 的转化率为70% |
| C.实验2 达平衡时,a<7.0 |
| D.实验3 达平衡后,再充入1.0molH2,K 值增大,平衡逆向移动 |
空气吹出法是工业规模海水提溴的常用方法,流程如下:
下列说法不正确的是:
A.步骤①中发生的主要反应为 |
| B.步骤②③的目的是富集溴元素 |
| C.物质X 为HBrO |
| D.空气吹出法用到了溴易挥发的性质 |