A、B、C和D等4种元素,A元素所处的周期数、主族序数、原子序数均相等;B的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层少2个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C。
(1)B在周期表中的位置第 周期,第 族;
(2)A、B形成的化合物的电子式 ;
(3)C的元素名称___ _____,C的最高价氧化物的化学式 ;
(4) D的最高价氧化物对应的水化物的化学式 。
.有甲、乙、丙三种物质:


甲乙丙
(1)乙中含有的官能团的名称为____________________。
(2)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同):
其中反应I的反应类型是_________,反应II的条件是_______________,反应III的化学方程式为__________________________________(不需注明反应条件)。
(3)由甲出发合成丙的路线之一如下:
(a)下列物质不能与B反应的是(选填序号)。
a.金属钠 b.FeCl3 c.碳酸钠溶液 d.HBr
(b)C的结构简式为___________;丙的结构简式为。
(c)D符合下列条件的所有同分异构体种,任写其中一种能同时满足下列条件的异构体结构简式。
a.苯环上的一氯代物有两种
b.遇FeCl3溶液发生显色反应
c.能与Br2/CCl4发生加成反应
.某烃A的相对分子质量为84。回答下列问题:
(1)下列物质与A以任意比例混合,若总物质的量一定,充分燃烧消耗氧气的量不相等的是(填序号)________。
a.C7H12O2 b.C6H14c.C6H14O d.C7H14O3
(2)若烃A为链烃,与HBr加成后只能得到一种产物,且该烃的一氯代物只有一种。
①A的结构简式为________________;
②链烃A与Br2的CCl4溶液反应生成B,B与NaOH的醇溶液共热可得到D,D分子中无溴原子。请写出由B制备D的化学方程式:__________________;
③B与足量NaOH水溶液完全反应,生成有机物E,该反应的化学方程式:_______________________________;E与乙二醇的关系是_______________。
(3)若核磁共振氢谱显示链烃A有三组不同的峰,峰面积比为3:2:1,则A的名称为__________________。
(4)若A不能使溴水褪色,且其一氯代物只有一种,则A的结构简式为
按要求填空:
(1)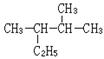 的系统命名为
的系统命名为
(2)松油醇(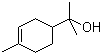 )的分子式为
)的分子式为
(3)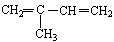 与Br2以物质的量之比为1:1反应,所得产物有种(不考虑顺反异构)
与Br2以物质的量之比为1:1反应,所得产物有种(不考虑顺反异构)
(4) 与新制的氢氧化铜在加热条件下反应的化学方程式
与新制的氢氧化铜在加热条件下反应的化学方程式
某有机物A,由C、H、O三种元素组成,在一定条件下,由A可以转化为有机物B、C和D、E;C又可以转化为B、A。它们的转化关系如下: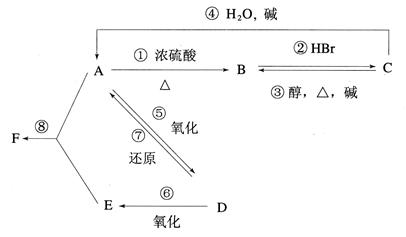
已知D的蒸气密度是氢气的22倍,并可以发生银镜反应。
⑴A~F的结构简式依次为____________、____________、____________、____________、____________、____________。
⑵在①~⑧的转化中属于消去反应的有____________加成反应的有____________取代反应的有____________。
⑶(在A~F中,选择适当的字母填空)适用于制作食品包装袋的单体是__________。常温下能与新制Cu(OH)2反应的是_______________,目前提倡用于和汽油按一定比例混合作汽车发动机燃料的是________________。
(4)分别写出①⑤的化学方程式。
请根据官能团的不同对下列有机物进行分类。(将序号填入空格处)(共8分)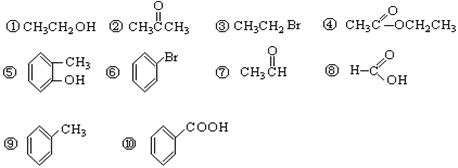
(1)芳香烃:;(2)卤代烃:;(3)醇:
(4)酚:;(5)醛:;(6)酮:
(7)羧酸:;(8)酯:。