根据以下实验事实,判断四种微粒在酸性条件下,氧化性由强到弱的顺序是( )
①向FeCl3溶液中滴加KI溶液,再加入CCl4振荡,CCl4层呈紫红色
②向FeCl2溶液中加入氯水,再加入KSCN溶液呈红色
③向KMnO4溶液中加入浓盐酸后,振荡后紫色褪去
| A.I2>Cl2>Fe3+>MnO | B.MnO>Cl2>Fe3+>I2 |
| C.Cl2>I2>Fe3+>MnO | D.Fe3+>MnO>Cl2>I2 |
工业上常将铬镀在其他金属表面,同铁、镍组成各种性质的不锈钢,在下图装置中,观察到图1装置铜电极上产生大量的无色气泡,而图2装置中铜电极上无气体产生,铬电极上产生大量有色气体,则下列叙述正确的是()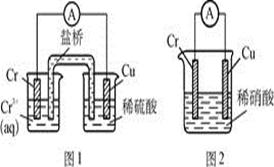
| A.图1为原电池装置,Cu电极上产生的是O2 |
| B.图2装置中Cu电极上发生的电极反应式为:Cu-2e-= Cu2+ |
| C.由实验现象可知:金属活动性Cu>Cr |
| D.两个装置中,电子均由Cr电极流向Cu电极 |
关于元素周期表,下列叙述中不正确的是()
| A.在金属元素与非金属元素的分界线附近可以寻找制备半导体材料的元素 |
| B.在过渡元素中可以寻找制备催化剂及耐高温和耐腐蚀的元素 |
| C.在非金属元素区域可以寻找制备新型农药材料的元素 |
| D.在地球上元素的含量的分布和它们在元素周期表中的位置有密切关系 |
下列表示物质结构的化学用语或模型图正确的是( )
A.氯化铵(NH4Cl)的电子式: |
B.H2O2的电子式: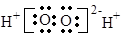 |
| C.HClO的结构式:H-O-Cl |
D.14C的原子结构示意图: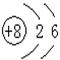 |
.下列各组微粒中,核外电子总数相等的是( )
| A.K+和Na+ | B.CO2和NO2 |
| C.CO和CO2 | D.N2和CO |
关于化学键的下列叙述中正确的是( ).
| A.离子化合物可能含共价键 | B.共价化合物可能含离子键 |
| C.离子化合物中只含离子键 | D.离子化合物不能含共价键 |