甘油三油酸脂是一种典型的脂肪,当它在人体内代谢时发生下列反应C57H104O6(s)+ 80 O2(g)= 57CO2(g)+52H2O(l)△H=" -3.35×10" 4 kJ·mol-1问如以高中男生平均每人每日耗能10125.3kJ,且以完全消耗这种脂肪来计算,每天需消耗甘油三油酸脂约( )
| A.1.2mol | B.0.6mol | C.0.3mol | D.0.15mol |
质谱图表明某有机物的相对分子质量为70,红外光谱表征到C=C和C=O的存在,1H核磁共振谱如下图(峰面积之比依次为1:1:1:3),下列说法正确的是
| A.分子中共有5种化学环境不同的氢原子 |
| B.该物质的分子式为C4H8O |
| C.该有机物的结构简式为CH3CH=CHCHO |
| D.在一定条件下,1mol该有机物可与3mol的氢气加成 |
下列说法正确的是
A.若完全燃烧,1 mol雄酮(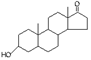 )比雌酮( )比雌酮(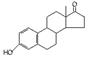 )多消耗2 mol O2 )多消耗2 mol O2 |
| B.苯分子中的一个碳原子被一个氮原子代替,则新分子的式量为79 |
| C.蔗糖、麦芽糖和乳糖的分子式都为C12H22O11,均能发生银镜反应 |
| D.只用溴水一种试剂不能鉴别甲苯、己烯、乙醇、四氯化碳四种液体 |
已知化合物B3N3H6(硼氮苯)与C6H6(苯)的分子结构相似,如右图。则硼氮苯的二氯取代物B3N3H4Cl2的同分异构体的数目为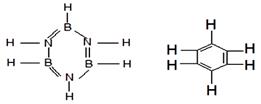
| A.6 | B.4 | C.3 | D.2 |
由两种烃组成的混合气体2L与足量的氧气充分反应后生成CO2 5L、H2O 7L(所有体积都在120℃测定),则这两种混合气体的可能组成是
| A.C2H4、C3H8 | B.CH4、C5H8 | C.CH4、C4H8 | D.C2H6、C3H8 |
为提纯下列物质(括号内为杂质),所用的除杂试剂和分离方法都正确的是
| 序号 |
不纯物 |
除杂试剂 |
分离方法 |
| A |
CH4(乙烯) |
酸性KMnO4溶液 |
洗气 |
| B |
溴乙烷(Br2) |
NaOH溶液 |
分液 |
| C |
乙醇(乙酸) |
饱和Na2CO3溶液 |
分液 |
| D |
C2H5OH(H2O) |
新制生石灰 |
蒸馏 |