下列实验能成功的是
| A.苯与浓溴水反应(Fe作催化剂)制溴苯 |
| B.乙醇、冰醋酸、稀硫酸共热制乙酸乙酯 |
| C.氯乙烯加聚后的生成物使酸性KMnO4溶液褪色 |
| D.甲酸甲酯能使新制Cu(OH)2在加热条件下产生红色沉淀 |
某有机物加氢反应后生成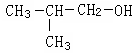 ,该有机物不可能是
,该有机物不可能是
| A.CH2="C" (CH3)CH2OH | B.(CH3)2CHCHO |
| C.CH3CH2CH2CHO | D.CH2="C" (CH3)CHO |
下列各组物质中,只用溴水就能鉴别的一组是
| A.甲烷、乙烯、丙烯 | B.苯、甲苯、二甲苯 |
| C.甲醇、乙醇、苯酚 | D.己烯、苯、苯酚 |
下列物质既能使酸性高锰酸钾溶液褪色,又能使溴水褪色,还能和氢氧化钠溶液反应的是
| A.乙酸 | B.乙酸甲酯 | C.丙烯酸甲酯 | D.苯甲酸 |
下列物质既能与金属钠反应放出气体,又能与纯碱作用放出气体的是
| A.CH3CH2OH | B.H2O | C.CH3COOH | D.C6H12O6(糖) |
不可能是乙烯加成产物的是
| A.CH3CH3 | B.CH3CHCl2 | C.CH3CH2OH | D.CH3CH2Br |