最近,“铬超标胶囊”事件引起社会强烈关注。铬的毒性与其价态及含量有关。铬常用作合金的生产原料,铬元素也是哺乳动物所需的微量元素之一。下图是铬在元素周期表中的相关信息,请回答:
(1)铬原子的核电荷数是 ;其相对原子质量为 。
(2)酒精监测仪中的反应原理为:C2H5OH+4X(红棕色)+ 6H2SO4 ="==2" Cr2 (SO4)3(绿色) + 2CO2↑+ 9H2O,则物质X的化学式为 ;Cr2 (SO4)3中Cr的化合价为 。
(3)据此信息,就物质或元素的安全性谈谈你的看法: 。
荔枝是很多人喜爱的水果,其中含有丰富的营养成分,如下表所示。请回答: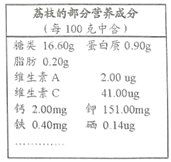
(1)表中钙、铁、硒等指的是 (填字母序号)。
| A.原子 | B.分子 | C.单质 | D.元素 |
(2)人体如果缺乏维生素C会诱发坏血病。每100g荔枝中含维生素C 的质量是 ug。
(3)表中所列荔枝含有的营养素共有 种,其中能为人体提供能量的物质是 (任答一种)。一个成年人一天约需要2000千卡能量,若其中有7%来自于荔枝(每100g荔枝的热量是70千卡),他一天最少应吃荔枝 g。
邓小平同志故居果山村盛产枇杷,有“枇杷之乡”之美誉。下图是这种枇杷的部分营养成分,请据图回答:
(1)图中的钙、钾、磷是指__________。
A.分子 B.原子C.元素 D.单质
(2)图中出现了六大营养素中的________类,能提供能量的营养素有__________种。
(3)糖类、蛋白质、脂肪都属于__________(填“有机物”或“无机物”)。
(4)枇杷适宜生长在pH为6左右的土壤中。若某土壤的pH为3 ,经改良后可种植枇杷。下列物质,既可用来改良土壤酸性,又能给土壤施肥的物质是____________。
A.生石灰
B.熟石灰
C.过磷酸钙
D.草木灰(主要成分碳酸钾)
酱油是中国的传统调味品,佛山海天酱油享誉国内外。下表是某酱油膏的部分营养成分列表,根据所学知识回答。
酱油膏的部分营养成分列表(每100克中含)
| 成分名称 |
含量 |
成分名称 |
含量 |
成分名称 |
含量 |
| 水分(克) |
54.7 |
蛋白质(克) |
13 |
脂肪(克) |
0.7 |
| 糖类(克) |
10.2 |
钠(毫克) |
7700 |
钙(毫克) |
46 |
| 铁(毫克) |
8.6 |
硒(微克) |
2.96 |
(1)上表中不含六大基本营养素中的 。
(2)上表中“钠”、“钙”等是指 (填“单质”、“分子”、“原子”或“元素”)。
(3)老年人每天都要摄入足量的钙,有利于防止 。
(4)糖类主要是给人体提供能量。写出葡萄糖(C6H12O6)在酶作用下缓慢氧化的化学方程式 。
(5)人体缺硒可能引起表皮角质化和癌症,但摄入量过高又会使人中毒。这里告诉人们的道理是 。
化学与人类生活密不可分。
(1)人们通过食物获取各种营养。
①水果和蔬菜富含的营养素主要有水和 。
②下列食物中,能提供大量蛋白质的是 (填字母序号)。
(2)下列厨房用品所使用的主要材料,属于有机合成材料的是 (填字母序号)。
(3)人类以化石燃料为主要能源。
①天然气燃烧的化学方程式为 。
②下列做法有利于减少空气污染的是 (填字母序号)。
| A.充分利用太阳能 | B.大力发展火力发电 |
| C.逐步加大清洁能源的比例 | D.为方便出行,大量使用私家车 |
I.随着人们对身体健康、生活质量的关注程度不断提高,越来越多的人喜爱上了既可以锻炼身体,又可以欣赏自然美景,还可以愉悦身心的爬山活动,成为众多“驴友”中的一员。
(1)“驴友”们在爬山时经常带的食品之一是牛肉,牛肉可为人体提供的营养素是 。
(2)爬山时,人体会大量出汗。你建议驴友还应带上适量的 (填字母)
A.糖盐水 B.果汁 C.巧克力
(3)晚间要使篝火燃烧的旺盛,其方法是 。
II.随着世界人口的增长,人类对粮食的需求量不断增大。俗话说,“庄稼一枝花,全靠肥当家。”请根据所学的知识,回答下列问题:
(1)农作物生长过程中,需求量最大的三种营养元素是 (填元素符号)。
(2)某农民发现自己地里的庄稼叶色枯黄,并且有部分倒伏现象,你建议它应该施用下列哪一种肥料最好 。
A.NH4ClB.K2SO4C.KNO3D.Ca(H2PO4)2
(3)用一种试剂即可鉴别NH4Cl和K2SO4这两种化学肥料,这种试剂是 (填化学式)。