下面的排序错误的是( )
| A.硬度由大到小:金刚石>碳化硅>晶体硅 |
| B.熔点由高到低:Al >Mg>Na |
| C.晶格能由大到小: NaF> NaCl> NaBr>NaI |
| D.氯的各种含氧酸的酸性由强到弱排列为HClO>HClO2>HClO3>HClO4 |
将0.1mol两种气体烃组成的混合气完全燃烧后得3.36L(标况)CO2和3.6g水,对于组成判断正确的是()
| A.一定有甲烷 | B.一定有乙烯 |
| C.一定没有甲烷 | D.一定有乙烷 |
下列化合物均为天然萜类化合物: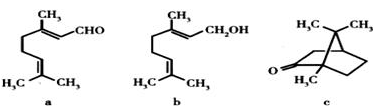
对这些萜类化合物叙述错误的是
| A.a和c互为同分异构体 | B.a和b互为同系物 |
| C.a、b能与溴水反应 | D.一定条件下b能转化为a |
向某溶液中逐滴加入0.5mol/L的NaOH溶液,生成沉淀的质量和加入NaOH溶液的体积之间的关系如下图所示 ,则该溶液中可能存在的离子是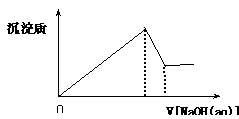
| A.只有Mg2+ | B.只有Al3+ |
| C.有H+、Mg2+和Al3+ | D.有Mg2+和Al3+ |
将c(H+)=10-2mol・L-1的醋酸和盐酸分别稀释100倍,稀释后两种溶液的c(H+)分别为a和
b,则a和b的关系为 ()。
| A.a>b | B.a<b | C.a=b | D.无法判断 |
美国康乃尔大学的魏考克斯(C. Wilcox)所合成的一种有机分子,就像一尊释迦牟尼佛,因而称为释迦牟尼分子,有关该有机分子的说法正确的是: ( ) 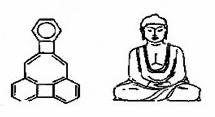
A.该有机物所有原子一定在同一平面 B.该有机物属于苯的同系物
C.该有机物分子中含有21个碳原子 D.该有机物一氯代物只有4种