汽车的启动电源常用铅蓄电池,放电时的电池反应如下:PbO2 + Pb + 2H2SO4 = 2PbSO4+ 2H2O,根据此反应判断下列叙述中正确的是( )
| A.PbO2是电池的负极 |
B.负极的电极反应式为:Pb + SO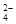 -2e– = PbSO4 -2e– = PbSO4 |
| C.PbO2得电子,被氧化 |
| D.电池放电时,溶液酸性增强 |
氢镍电池是近年开发出来的可充电电池,它可以取代会产生镉污染的镉镍电池。氢镍电池的总反应式是1/2H2+NiO(OH) Ni(OH)2,根据此反应式判断,下列叙述正确的是
Ni(OH)2,根据此反应式判断,下列叙述正确的是
| A.电池放电时,电池负极周围溶液的pH不断增大 |
| B.电池放电时,镍元素被氧化 |
| C.电池放电时,氢元素被还原 |
| D.电池放电时,H2是负极 |
用惰性电极实现电解,下列说法正确的是
| A.电解稀硫酸溶液,实质上是电解水,故溶液pH不变 |
| B.电解稀氢氧化钠溶液,要消耗OH-,故溶液pH减小 |
| C.电解硫酸钠溶液,在阴极上和阳极上析出产物的物质的量之比为1∶2 |
| D.电解氯化铜溶液,在阴极上和阳极上析出产物的物质的量之比为1∶1 |
用滴有酚酞和氯化钠试液的湿润滤纸分别做甲、乙两个实验,能发现附近变成红色的电极是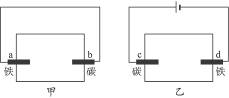
| A.ac | B.bd | C.ad | D.bc |
下图X、Y分别是直流电源的两极,通电后发现a极板质量增加,d极板有无色无臭气体放出,符合这一情况的是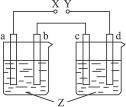
| A极板 |
d极板 |
X电极 |
Z溶液 |
|
| A |
锌 |
石墨 |
负极 |
CuSO4 |
| B |
石墨 |
石墨 |
负极 |
NaOH |
| C |
银 |
铁 |
正极 |
AgNO3 |
| D |
铜 |
石墨 |
负极 |
CuCl2 |
用惰性电极电解下列溶液,电解一段时间后,阴极质量增加,电解溶液的pH下降的是
| A.CuCl2 | B.AgNO3 | C.BaCl2 | D.H2SO4 |