COCl2(g) 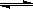 CO(g)+Cl2(g) △H>0,当反应达到平衡时,下列措施①升温②恒容通入惰性气体③增加CO的浓度④减压⑤加催化剂⑥恒压时通入惰性气体,能提高COCl2转化率的是( )
CO(g)+Cl2(g) △H>0,当反应达到平衡时,下列措施①升温②恒容通入惰性气体③增加CO的浓度④减压⑤加催化剂⑥恒压时通入惰性气体,能提高COCl2转化率的是( )
| A.①②④ | B.①④⑥ | C.②③⑥ | D.③⑤⑥ |
下列物质的熔、沸点高低顺序正确的是
| A.金刚石>晶体硅>二氧化硅>碳化硅 | B.CI4>CBr4>CCl4>CH4 |
| C.MgO>H2O>O2>NH3 | D.金刚石>生铁>纯铁>钠 |
已知:2CO(g)+O2(g)=2CO2(g)ΔH="-566" kJ/mol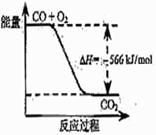

 Na2O2(s)+CO2(g)=Na2CO3(s)+
Na2O2(s)+CO2(g)=Na2CO3(s)+ 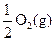 ΔH="-226" kJ/mol
ΔH="-226" kJ/mol 根据以上热化学方程式判断,下列说法正确的是
根据以上热化学方程式判断,下列说法正确的是 A.CO的燃烧热为283 kJ
A.CO的燃烧热为283 kJ B.右图可表示由CO生成CO2的反应过程和能量关系
B.右图可表示由CO生成CO2的反应过程和能量关系 C.2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g)ΔH>-452 kJ/mol
C.2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g)ΔH>-452 kJ/mol D.CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为6.02×1023
D.CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为6.02×1023
在下列各溶液中,离子一定能大量共存的是

A.强碱性溶液中:K+、Al3+、Cl-、SO42- |
B.含有0.1 mol·L-1 Fe3+的溶液中:K+、Mg2+、I-、NO3- |
C.含有0.1 mol·L-1Ca2+溶液在中:Na+、K+、CO32-、Cl- |
D.室温下,pH=1的溶液中: Na+、Fe3+、NO3-、SO42- |
能正确表示下列反应的例子方程式是
| A.向次氯酸钙溶液通入过量CO2:Ca2++2ClO—+CO2+H2O =CaCO3↓+2HClO |
| B.向次氯酸钙溶液通入SO2:Ca2++2ClO—+SO2+H2O= CaSO3↓+2HClO |
| C.氢氧化钙溶液与碳酸氢镁溶液反应:HCO3—+Ca2++OH—=CaCO3↓+H2O |
| D.在氯化亚铁溶液中加入稀硝酸:3Fe2++4H++NO3—=3Fe3++NO↑+2H2O |
Fe(OH)3胶体和MgCl2溶液共同具有的性质有
| A.都比较稳定,密封放置不产生沉淀 | B.两分散系均有丁达尔现象 |
| C.加入盐酸先产生沉淀,随后溶解 | D.分散质微粒可通过半透膜 |