下列离子方程式书写错误的是
| A.向足量的NaHCO3溶液中逐渐滴入澄清石灰水:Ca2++2OH—+2HCO3- =2H2O+CaCO3↓+ CO32- |
| B.向足量的NaHSO4溶液中逐渐滴入Ba(HCO3)2溶液:Ba2++2H++2HCO3-+ SO42-=2H2O+BaSO4↓+2 CO2↑ |
| C.向饱和Na2CO3溶液中通入足量的CO2:CO32-+ CO2+ H2O="2" HCO3- |
| D.向NaHSO4溶液中逐渐滴入Ba(OH)2溶液至沉淀完全:H++ SO42-+ Ba2++ OH—= BaSO4↓+ H2O |
实验室进行NaCl溶液蒸发结晶时,一般有以下操作过程
①固定铁圈位置②放置酒精灯③放上石棉网④放上蒸发皿
⑤加热搅拌⑥停止加热.余热蒸干,其正确的操作顺序为
| A.①②③④⑤⑥ | B.②①③④⑤⑥ | C.②①④⑤⑥ | D.②①③④⑤ |
下列试纸在使用时不宜用水湿润的是
| A.蓝色石蕊试纸 | B.淀粉碘化钾试纸 | C.pH试纸 | D.红色石蕊试纸 |
某温度下,在容积固定不变的密闭容器中发生下列可逆反应:X(g) + 2Y(g) 2Z(g)。
2Z(g)。
平衡时,X、Y、Z的物质的量分别为1 mol、1 mol、2 mol,保持温度不变,再向容器中分别充入1 mol、1 mol、2 mol的X、Y、Z,则下列叙述中正确的是
| A.刚充入时,反应速率V (正)减小,V (逆)增大 |
| B.达到新平衡时,容器内气体的平均相对分子质量增大 |
| C.达到新平衡时,容器内气体的压强是原来的两倍 |
| D.达到新平衡时,容器内气体的百分组成和原来相同 |
pH=1的两种酸溶液A、B各1mL,分别加水稀释到1000mL,其pH与溶液 体积(V)的关系如图示,下列说法不正确的是
体积(V)的关系如图示,下列说法不正确的是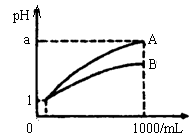
A.A、B两种酸溶液的物质的量浓度一定相等
B.稀释后,A酸溶液的酸性比B酸溶液弱
C.若a=4,则A是强酸,B是弱酸
D.若1<a<4,则A、B都是弱酸
放热反应CO(g)+H2O(g) 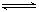 CO2(g)+H2(g)在温度t1时达到平衡,c1(CO)=c1(H2O)="1.0" mol·L-1,其平衡常数为K1。其他条件不变升高反应体系的温度至t2时,反应物的平衡浓度分别为c2(CO)和c2(H2O),平衡常数为K2,则
CO2(g)+H2(g)在温度t1时达到平衡,c1(CO)=c1(H2O)="1.0" mol·L-1,其平衡常数为K1。其他条件不变升高反应体系的温度至t2时,反应物的平衡浓度分别为c2(CO)和c2(H2O),平衡常数为K2,则
| A.若增大CO浓度,K2和K1都增大 | B.K2>K1 |
| C.c2(CO)=c2(H2O) | D.c1(CO)>c2(CO) |