下列说法正确的是( )
| A.相同物质的量的任何物质具有相同数目的微粒 |
| B.同物质的量浓度同体积的任何溶液中所含溶质微粒数目相同 |
| C.含58.5 克氯化钠的溶液中含有6.02×1023个氯化钠分子 |
| D.无论什么状况下,一定质量的某种气体含有的分子数是一定的 |
有一种瓦斯分析仪能够在煤矿巷道中的甲烷达到一定浓度时,通过传感器显示出来。该瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如下图所示,其中的固体电解质是Y2O3-Na2O,O2-可以在其中自由移动。下列有关叙述正确的是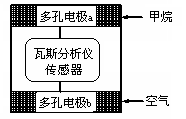
| A.电极a的反应式为:CH4+4O2--8e-=CO2+2H2O |
| B.电极b是正极,O2-由电极a流向电极b |
| C.瓦斯分析仪工作时,电池内电路中电子由电极a流向电极b |
| D.当固体电解质中有1 mol O2-通过时,电子转移4 mol |
下列溶液中微粒的物质的量浓度关系正确的是
A.常温下,pH=7的NH4Cl与氨水的混合溶液:c(H+)= c(OH-)= c(NH )=c(Cl-) )=c(Cl-) |
| B.0.1 mol/L Na2S溶液:c(OH-)=c(H+)+c(HS-)+c(H2S) |
| C.pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1 |
| D.常温下,pH=2的CH3COOH与pH=12的NaOH等体积混合:c (CH3COO-)+ c(H+)>c(Na+)+c(OH-) |
酚酞,别名非诺夫他林,是制药工业原料,其结构如图所示,有关酚酞说法不正确的是
| A.分子式为C20H14O4 |
| B.可以发生取代反应、加成反应、氧化反应 |
| C.含有的官能团有羟基、酯基 |
| D.1 mol该物质可与H2和溴水发生反应,消耗H2和Br2的最大值为10 mol和4 mol |
下列解释实验事实的化学方程式或离子方程式正确的是
A.用pH试纸检测,氨水溶液呈碱性: NH3·H2O  NH4++OH— NH4++OH— |
B.100 ℃时,测得纯水中c(H+)·c(OH—) =1×10—12:H2O(l) H+(aq)+OH—(aq) H+(aq)+OH—(aq) H<0 H<0 |
C.FeCl3溶液中通入适量SO2,溶液黄色褪去:2Fe3++SO2 +2H2O  2Fe2++SO42—+ 4H+ 2Fe2++SO42—+ 4H+ |
| D.向苯酚钠溶液中通入CO2,溶液变浑浊:2C6H5ONa+CO2+H2O →2C6H5OH+Na2CO3 |
下表中各组物质之间不能通过一步反应实现下图转化的是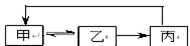
| 甲 |
乙 |
丙 |
|
| A |
AlCl3 |
Al(OH)3 |
Al2O3 |
| B |
SiO2 |
H2SiO3 |
Na2SiO3 |
| C |
Cl2 |
HCl |
NaCl |
| D |
CH2=CH2 |
CH3CH2Cl |
CH3CH2OH |