如图是两种物质的溶解度曲线,回答下列问题:
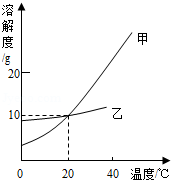
(1)20℃时,甲物质的溶解度是
.
(2)20℃时,甲物质的饱和溶液中,溶质和溶剂的质量比为.
(3)将40℃时的乙物质的饱和溶液变为不饱和溶液,可采用的方法是(写一张即可).
(4)40℃时,将甲、乙两种物质的饱和溶液分别降温到20℃,所得溶液的溶质质量分数的大小关系是.
(5)甲的热饱和溶液中含有少量的乙,若提纯甲,可采用法(填"冷却结晶"或"蒸发结晶").
如图是化肥碳酸氢铵(
)标签的部分内容。
⑴纯净的
3由种元素组成,其中
元素的质量分数为;则上述碳到氢铵化肥属于(填"纯净物"或"混合物");
⑵根据碳酸氢铵的保存和施用注意事项推测,其物理性质是,化学性质是。(各填一条即可)
“西气东输”工程使我省很多地区都用上了天然气(主要成分CH4)。实验室常用图1所示的发生装置制取CH4,回答下列问题。 
(1) 图1中仪器a的名称是______________。
(2)实验室可用_______________方法收集CH4
(3)天然气不完全燃烧会产生一种有毒气体,其化学式为__________。因此,使用热水器时,防止发生中毒的做法是________________(写出一种即可)
(4)充分燃烧1kg不同化石燃料所产生CO2和SO2气体的质量如图2 所示,则--------------燃烧最易导致酸雨,————————————燃烧对环境影响最小。
如图为某抗酸药的实物图,回答下列问题。
(1)图中标示的物质中,含义的金属元素是_______(写出一种即可),属于有机合成材料的是_______________
(2)淀粉属于——————————————(填字母序号)。
| A.蛋白质 | B.糖类 | C.油 脂 | D.维生素 |
(3)图中塑料包装废弃后可用于微型实验。如鉴别氢氧化镁和碳酸氢钠(均可作抗酸药)两种白色粉末时,可分别取少量样品放入废弃包装的两个孔穴中,再滴入————————(填试剂名称),有————————————————————现象的原物质是碳酸氢钠。
(4)另一种抗酸药的主要成分是三硅酸镁(Mg2Si3O8·nH2O),能与盐酸发生复分解反应,则反应后产物中含镁的化合物是——————————————(填化学式)。
中安在线2011年2月15日报道,安徽滁洲正在以石英资源为基础,打造培育千亿元硅产业。石英的主要成分为二氧化硅,它是玻璃工业和陶瓷工业的原料,冶金工业的助熔剂。
(1)二氧化硅的结构与金刚石相似,都是由(填“分子”、“原子”、或“离子”)构成的,二氧化硅属于(填“酸”、“碱”、“盐”或“氧化物”)。
(2)装有氢氧化钠溶液的试剂瓶不能用玻璃塞,原因是在常温下,NaOH与玻璃塞中的SiO2缓慢地发生反应生成Na2SiO3和H2O。Na2SiO3使瓶口与瓶塞粘合在一起,则该反应的化学方程式为。
(3)硅是太阳能电池和电脑芯片不可缺少的材料。生产高纯硅的流程示意图如下:
① 制备粗硅的反应为:SiO2 + 2C Si + 2CO↑,反应的基本类型是
Si + 2CO↑,反应的基本类型是
② 整个制备过程必须达到无水无氧,若在H2还原SiHCl3过程中混入O2,可能引起的后果是。
③ 为了达到绿色化学和节约资源的目的,物质A需要循环使用,A的化学式是
某化学兴趣小组在刷洗试管时,用力过猛。造成试管底被穿通,留下圆形小孔。在老师的启发下。兴趣小组变废为宝,将细铜丝揉成小球垫在试管底部,配上带单孔橡皮塞的导管和烧杯,装配了一个在实验室制取气体的装置,如图所示。
(1)若用此装置制取二氧化碳,在试管内的铜丝球上方应盛放块状__________ (填药品名称。下同),发生反应的化学方程式 ________________________________________;若用此装置制取氢气.在试管内的铜丝球上方应盛放__________发生反应的化学方程式______________________________。
(2)制备气体之前,都必须要捡查装置的气密性。写出你检查该装置气密性的方法:
______________________ 。