短周期元素的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则叙述正确的是
| A.原子半径A>B>D>C | B.原子序数d>c>b>a |
| C.离子半径C>D>B>A | D.单质的还原性A>B>D>C |
对可逆反应4NH3(g)+ 5O2(g) 4NO(g)+ 6H2O(g),下列叙述正确的是
4NO(g)+ 6H2O(g),下列叙述正确的是
| A.达到化学平衡时,4υ正(O2)= 5υ逆(NO) |
| B.若单位时间内生成x mol NO的同时,消耗x mol NH3 ,则反应达到平衡状态 |
| C.达到化学平衡时,若增加容器体积,则正反应速率减少,逆反应速率增大 |
| D.化学反应速率关系是:2υ正(NH3)= 3υ正(H2O) |
已知反应A2(g)+2B2(g) 2AB2(g)的△H<0,下列说法正确的
2AB2(g)的△H<0,下列说法正确的
| A.升高温度,正向反应速率增加,逆向反应速率减小 |
| B.升高温度有利于反应速率增加,从而缩短达到平衡的时间 |
| C.达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动 |
| D.达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动 |
反应:L(固)+aG(气)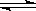 bR(气)达到平衡时,温度和压强对该反应的影响如图所示:压强p1>p2, x轴表示温度,y轴表示平衡混合气中G的体积分数。据此可判断
bR(气)达到平衡时,温度和压强对该反应的影响如图所示:压强p1>p2, x轴表示温度,y轴表示平衡混合气中G的体积分数。据此可判断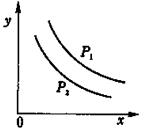
A.上述反应是放热反应 B.上述反应是吸热反应
C. 1+a >b D.1+a <b
1+a >b D.1+a <b
对于可逆反应 2AB3(g) 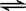 A2(g) + 3B2(g),△H>0;下列图像正确的是
A2(g) + 3B2(g),△H>0;下列图像正确的是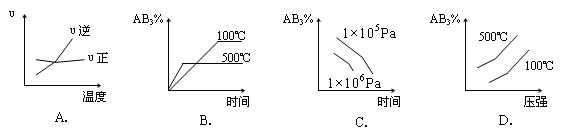
在一定温度不同压强(P1<P2)下,可逆反应2X(g) 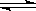 2Y(g) + Z(g)中,生成物Z在反应混合物中的体积分数(ψ)与反应时间(t)的关系有以下图示,正确的是
2Y(g) + Z(g)中,生成物Z在反应混合物中的体积分数(ψ)与反应时间(t)的关系有以下图示,正确的是