元素周期表中,一稀有气体元素原子的最外层电子构型为4s24p6,与其同周期的A、B、C、D四种元素,它们的原子最外层电子数依次为2、2、1、7,其中A、C两元素原子的次外层电子数为8,B、D两元素原子的次外层电子数为18,E、D两元素处于同族,且在该族元素中,E的气态氢化物的沸点最高。
(1)B元素在周期表中的位置 ; D的最高价氧化物的水化物的化学式为______。
(2)E的气态氢化物在同族元素中沸点最高的原因是: 。
(3)A、C两元素第一电离能前者 后者(填“大于”或“小于”)。无论是A和C的单质还是A和C的氢化物的固体,均能与水剧烈反应生成气体,当上述四种固体分别与足量水反应时,满足n(消耗固体):n(气体):n(转移电子)=1:1:1关系的反应的化学方程式_______________。
(4)B元素能形成多种配合物,如B2+可与NH3形成配离子[B(NH3)4]2+。其配体的空间构型为 ;右图表示B与某种元素X形成的化合物晶胞,如果该化合物中B和X通过离子键结合,该晶体中阳离子的配位数为 。若B和X通过共价键结合,则该化合物的化学式为 (a ZnX b ZnX2 c ZnX3)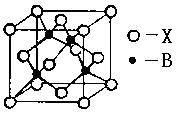
(5)A和E可形成离子化合物,其晶胞结构如图示。该化合物的电子式_______。则晶胞中与A离子距离相等且最近的E离子围成的几何体形状是_______。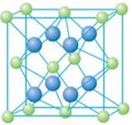
下表是元素周期表一部分,列出了九种元素在周期表中的位置:
| 族 周期 |
IA |
IIA |
IIIA |
IVA |
VA |
VIA |
VIIA |
0 |
| 2 |
⑤ |
⑥ |
⑦ |
⑧ |
||||
| 3 |
① |
③ |
④ |
⑨ |
||||
| 4 |
② |
请用化学用语回答下列问题
(1)在上述元素中,金属性最强的是,在③~⑦元素中,原子半径最大的是;
(2)①~⑨中元素最高价氧化物对应的水化物中酸性最强的是(填物质化学式)。写出①和④的最高价氧化物对应的水化物反应的离子方程式。
(3)用电子式表示③和⑨形成的化合物的形成过程。
(4)表中元素①和⑦可以形成一种淡黄色物质X,写出X的电子式:,该物质所含化学键类型,0.1mol X与水反应转移电子数为:。
(5)表中元素⑥和⑧可形成一种相对分子量为66的共价化合物Y,Y分子中各原子均达到“8电子稳定结构”,Y的结构式。
A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。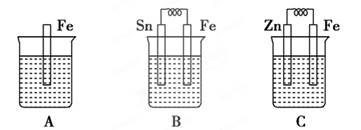
(1)分别写出B、C装置中铁片表面发生的电极反应:
B:________________________________________
C:________________________________________
(2)A、B、C中铁被腐蚀的速率,由快到慢的顺序是_____________
(3)科学工作者为心脏病人设计的心脏起搏器的电池是以Pt和Zn为电极材料,依靠人体内液体中含有一定浓度的溶解氧、H+和Zn2+进行工作。该电池的正极反应:。
按要求填写下列空格。
(1)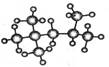 的分子式为:,其一氯代物有种,该烃有多种同分异构体,其中有一种一氯取代物只有一种,写出这种同分异构体的结构简式:
的分子式为:,其一氯代物有种,该烃有多种同分异构体,其中有一种一氯取代物只有一种,写出这种同分异构体的结构简式:
(2)分子式为C6H14的烃的主链为4个碳的同分异构体共有种。
(3)写出实验室制取硝基苯的化学方程式:。
(每空2分,共16分)环己烯常用于有机合成。现通过下列流程,以环己烯为原料合成环醚、聚酯、橡胶,其中F可以作内燃机的抗冻剂,J分子中无饱和碳原子。
已知:R1-CH=CH-R2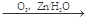 R1-CHO+R2-CHO
R1-CHO+R2-CHO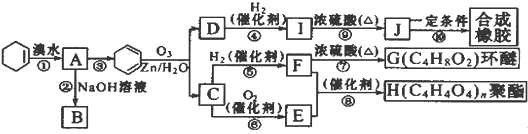
(1)A分子中若有一个氢原子被溴原子取代,则取代产物有种。F的名称是,C中含有的官能团的名称是。
(2)③的反应条件是。
(3)写出下列反应类型:⑥,⑨。
(4)有机物B和I的关系为(填序号,多填扣分)。
| A.同系物 | B.同分异构体 | C.都属于醇类 | D.都属于烃 |
(5)写出反应⑩的化学方程式:。
(每空2分,共14分)美国化学家R.F.Heck因发现Heck反应而获得2010年诺贝尔化学奖。例如经由Heck反应合成一种防晒剂:
反应①: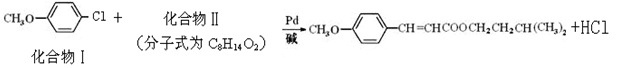
化合物Ⅱ可由以下合成路线获得:
(1)化合物I核磁共振氢谱显示存在组峰,化合物I的分子式为。
(2)1mol化合物Ⅱ完全燃烧最少需要消耗mol O2,其完全水解的化学方程式为(注明条件)。
(3)化合物Ⅲ中含氧官能团的名称是;化合物Ⅴ与浓H2SO4共热生成化合物Ⅵ,化合物Ⅵ能使酸性KMnO4溶液褪色,化合物Ⅵ的结构简式是。
(4)化合物Ⅰ的一种同分异构体化合物Ⅶ符合下列条件:苯环上有两个取代基且苯环上只有两种不同化学环境的氢,与FeCl3溶液作用显紫色。化合物Ⅶ与过量NaOH溶液共热,发生反应的方程式为。