某化学教师为“氯气与金属钠反应”设计了如图装置与操作以替代相关的教材上的实验。实验操作:先给钠预热,当钠熔成圆球时,撤火、通入氯气,即可见钠着火燃烧,并产生大量白烟。以下叙述错误的是( )
| A.钠着火燃烧产生苍白色火焰 |
| B.反应生成的大量白烟是氯化钠晶体 |
| C.管中部塞一团浸有NaOH溶液的棉球是用于吸收过量的氯气,以免其污染空气 |
| D.管右端棉球外颜色变化可判断氯气是否被碱液完全吸收 |
下列反应中生成物总能量高于反应物总能量的是
| A.氢氧化钠溶液与稀盐酸混合 | B.氢氧化钡晶体与氯化铵晶体混合搅拌 |
| C.乙醇燃烧 | D.铝热反应 |
下列不正确的是
| A.非金属性:F>O>S | B.金属性:Rb>K>Li |
| C.稳定性:PH3>H2S>HCl | D.碱性:NaOH>Mg(OH)2>Al(OH)3 |
有关化学用语正确的
| A.乙烯的结构简式:CH2CH2 |
B.四氯化碳的电子式: |
C.甲烷分子的比例模型: |
| D.HClO的结构式:H-Cl-O |
今年世界环境日中国主题为“践行绿色生活”, 该主题旨在增强全民环境意识、节约意识、生态意识,选择低碳、节俭的绿色生活方式和消费模式,形成人人、事事、时时崇尚生态文明的社会新风尚,为生态文明建设奠定坚实的社会和群众基础。下列不符合这一主题的是
| A.建立合法、公开的地沟油回收生产制度,将生产的地沟油用作工业用油。 |
| B.将生活垃圾分类回收、加工、使之再生、再利用。 |
| C.生活污水、工业废水不要乱排放,通过打深井,将之排到地层深处。 |
| D.不用一次性筷子、不浪费纸张、不浪费粮食、做“光盘”一族。 |
普伐他汀是一种调节血脂的药物,其结构如图所示(未表示出其空间构型)。下列关于普伐他汀的性质描述正确的是 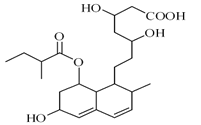
| A.不能通过反应形成高分子化合物 | B.不能使酸性KMnO4溶液褪色 |
| C.能发生加成、取代、消去反应 | D.1mol该物质最多可与1molNaOH反应 |