一定条件的密闭容器中:4NH3(g)+5O2(g) 4NO(g)+6H2O(g) ΔH=-905.9 kJ·mol-1,下列叙述不正确的是
4NO(g)+6H2O(g) ΔH=-905.9 kJ·mol-1,下列叙述不正确的是
| A.达到平衡时放出热量为905.9 kJ,则起始时投入4 mol NH3和5 mol O2 |
| B.平衡时4v正(O2)=5v逆(NO) |
| C.平衡后降压,混合气体平均摩尔质量减小 |
| D.NH3与O2起始时物质的量之比等于4:5,则平衡后两物质的转化率一定相等 |
下列叙述正确的是( )
| A.分子晶体中的每个分子内一定含有共价键 |
| B.原子晶体中的相邻原子间只存在非极性共价键 |
| C.离子晶体中可能含有共价键 |
| D.金属晶体的熔点和沸点都很高 |
某3克醛和足量的银氨溶液反应,结果析出43.2克Ag,则该醛为()
| A.甲醛 | B.乙醛 | C.丙醛 | D.丁醛 |
某有机样品3.1克完全燃烧,燃烧后的混合物通入过量的澄清石灰水中,盛石灰水的烧杯共增重7.1克,经过滤得到10克沉淀。该有机样品可能是()
| A.乙醚 | B.乙醇 | C.乙醛 | D.甲醇和丙三醇的混合物 |
近两年流行喝苹果醋,苹果醋是一种由苹果发酵而成的具有解毒、降脂、减肥和止泻等明显药效的健康食品。苹果酸(α—羟基丁二酸)是这种饮料的主要酸性物质,苹果酸的结构简式为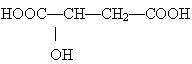 ,下列说法不正确的是()
,下列说法不正确的是()
| A.苹果酸在一定条件下能发生酯化反应 |
| B.苹果酸在一定条件下能发生催化氧化反应 |
| C.苹果酸在一定条件下能发生消去反应 |
| D.1mol苹果酸与Na2CO3溶液反应最多消耗3mol Na2CO3 |
C8H8的分子呈正六面体结构,因而称为"立方烷",它的六氯代物的同分异构体共有( )
| A.3种 | B.6种 | C.12种 | D.24种 |