在全球气候变暖的背景下,以低能耗、低污染为基础的“低碳经济”成为发展趋向。下列不属于“促进低碳经济”宗旨的是( )
| A.提高能源效率、寻找替代能源、保护森林以及生态友好型消费 |
| B.推广以液化石油气代替天然气作民用燃料 |
| C.推广利用二氧化碳与环氧丙烷和琥珀酸酐的三元共聚物的生物降解材料 |
| D.推广“绿色自由”计划,吸收空气中CO2并利用廉价能源合成汽油 |
香柠檬油可用于化妆品。香柠檬油中含微量的香柠檬酚和香柠檬醚,其结构分别如图。下列说法不正确的是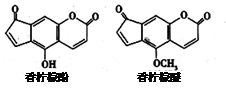
| A.香柠檬酚通过取代反应可转化为香柠檬醚 |
| B.1 mol香柠檬酚在NaOH溶液中水解时最多消耗2 mol NaOH |
| C.可用FeCl3溶液来鉴别香柠檬酚和香柠檬醚 |
| D.香柠檬酚和香柠檬醚均能与溴水反应,但反应类型不完全相同 |
下列对有机物的结构或性质的描述错误的是
| A.分别向蛋白质溶液中加入饱和(NH4)2SO4和CuSO4溶液均出现沉淀,但原理不同 |
| B.完全燃烧28 g乙烯和聚乙烯的混合物生成2 mol H2O |
| C.卤代烃水解、酯的水解反应中加入的NaOH都作催化剂 |
| D.肥皂水中分别加入硬水和稀硫酸,析出沉淀不相同 |
在一个容积为3 L的恒温密闭容器中,放入3 L X(g)和2 L Y(g),在一定条件下发生反应:4X(g) + 3Y(g) 2Q(g) + nR(g),反应达平衡后,容器内压强比原来增加5%,X的浓度减少1/3,则n值可能为
2Q(g) + nR(g),反应达平衡后,容器内压强比原来增加5%,X的浓度减少1/3,则n值可能为
| A.6 | B.5 | C.4 | D.3 |
实验过程中要特别注意操作步骤的先后顺序,下列先后顺序有错的是
| A.燃烧法测定有机物组成时先用碱石灰测CO2质量,再用浓H2SO4测H2O质量 |
| B.制硝基苯需要配制混合酸,应先加浓硝酸再加浓硫酸 |
| C.检验淀粉在稀硫酸作用下是否发生水解,应在水解液中先加入NaOH溶液中和后再加入银氨溶液共热 |
| D.检验丙烯醛(CH2=CH—CHO)中的官能团时,应先用新制Cu(OH)2试剂检验醛基再用KMnO4溶液检验碳碳双键 |
下列说法正确的是
| A.一定条件下,增大反应物的量会加快化学反应速率 |
| B.增大压强,肯定会加快化学反应速率 |
| C.活化分子间所发生的碰撞为有效碰撞 |
| D.能够发生有效碰撞的分子叫活化分子 |