某化学课外活动小组在调查一化工厂时发现该厂有甲、乙两个车间,排出的废水澄清透明,经分析分别含有三种不同的离子,共有K+、Ba2+、Cu2+、OH-、NO3-、CO32- 六种离子,经查部分物质的溶解性见下表:
| |
OH- |
NO3- |
CO32- |
| K+ |
溶 |
溶 |
溶 |
| Ba2+ |
溶 |
溶 |
不 |
| Cu2+ |
不 |
溶 |
不 |
(1)将甲、乙两车间的废水按适当比例混合,可以变废为宝,既能使废水中的Ba2+、Cu2+、OH-、CO32- 等离子转化为沉淀除去,又可以用上层清液来浇灌农田。清液中含有的溶质主要是 _______ (填写物质的化学式)。
(2)已知甲车间废水明显呈碱性,则乙车间废水中含有的阴离子是_______ 。
(3)根据以上溶解性表判断,Ba(NO3)2和K2CO3溶液 _______ (填“能”或“不能”)发生复分解反应。若能反应写出化学方程式,若不能反应写出理由:_______________________________。
下图中的①、②是氟元素、钙元素在元素周期表中的信息,A、B、C、D是四种粒子的结构示意图。
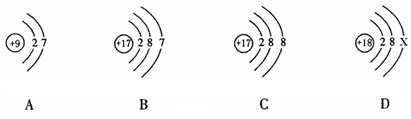
请你回答:
(1)氟元素的相对原子质量为,钙元素的原子序数为;
(2)X=;
(3)A、B、C、D属于同种元素的粒子是(填序号);
(4)A粒子的化学性质与B、C、D中哪一种粒子的化学性质相似(填序号)。
用数字和化学符号表示:
①2个氮气分子;②3个亚铁离子;
③亚硝酸钠中氮元素显+3价;④构成氯化钠的微粒_____、;
⑤“西气东输”工程所输送气体中的主要成分;⑥硫酸铝。
下面是碳的几种单质的结构示意图,图中小圆圈均代表碳原子。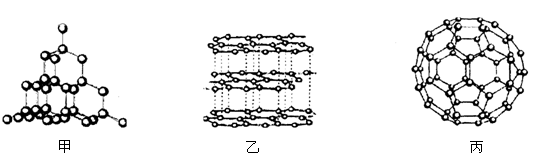
(1)在物质甲的结构中,每个碳原子最多连有______个碳原子。
(2)根据乙物质层与层之间能发生滑动,具有滑腻感的特点,写出它的一种用途_________。(3)图中物质丙的化学式为C60,已知硅的一种单质也有与物质丙相同的原子数和类似的结构,有科学家尝试把物质丙的一个分子放进硅的这种单质的一个分子中,反应形成一种新型分子,该分子的化学式为。
对知识的比较与归纳是学习化学的重要方法,现有以下三个化学方程式: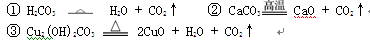
通过比较发现:(1)它们有许多相似之处,请写出其中的两条:
①;②。
(2)它们也有许多不同,请指出其中一个与另外两个的不同之处:
(答一条即可)。
如图,将几块经过烘烤并冷却后的木炭(或活性炭),投入到盛满红棕色二氧化氮气体的集气瓶中,轻轻摇动,红棕色逐渐消失,这是因为;倒扣的漏斗内水面(填“上升”、“下降”或“不变”)。