常温下,用0.10 mol·L-1 KOH溶液滴定10.00 mL 0.10 mol·L-1H2C2O4(二元弱酸)溶液所得滴定曲线如图(混合溶液的体积可看成混合前溶液的体积之和)。下列说法正确的是
| A.点①所示溶液中: c(H+)/c(OH—)=1012 |
| B.点②所示溶液中: c(K+)+c(H+)=c(HC2O4—)+c(C2O42-)+c(OH—) |
| C.点③所示溶液中:c(K+)>c(HC2O4—)> c(H2C2O4)>c(C2O42-) |
| D.点④所示溶液中:c(K+)+ c(H2C2O4)+ c(HC2O4—) +c(C2O42-)=0.10mol·L-1 |
下列物质中既能跟稀H2SO4反应, 又能跟氢氧化钠溶液反应的是 ()
①NaHCO3 ②Al2O3 ③Al(OH)3 ④Al
| A.③④ | B.②③④ | C.①③④ | D.全部 |
“垃圾是放错了位置的资源”,应该分类回收利用。生活中废弃的塑粒袋、医院的废输液管、废旧轮胎等可以归为一类加以回收利用。它们属于()
| A.糖类 | B.有机物 | C.氧化物 | D.盐 |
ClO2是新一代饮用水的消毒剂,许多发达国家的自来水厂采用ClO2代替CL2来进行自来水消毒。我国最近成功研制出制取CLO2的新方法,其反应的微观过程如下所示: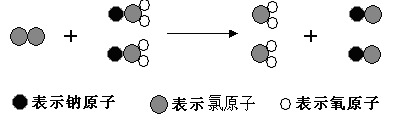
下列有关该反应的叙述中正确的是
| A.该反应是复分解反应 |
| B.该反应的化学方程式为Cl2+2NaClO2====2ClO2+2NaCl |
| C.反应中Cl2既是氧化剂,又是还原剂 |
| D.NaClO2和ClO2中Cl的化合价相同 |
饱和氯水长期放置后,下列微粒在溶液中不减少的是
| A.Cl2 | B.HClO | C.Cl- | D.H2O |
为了除去氯气中混有的少量水蒸气,可使含杂质的氯气通过某特定的干燥管,此干燥管中装有下列药品中的.
| A.五氧化二磷粉未 | B.浓硫酸 | C.饱和食盐水 | D.碱石灰 |