下列表述正确的是
| A.0.1mol·L-1Na2CO3溶液中:c(OH-)=c(HCO3-)+c(H+)+c(H2CO3) |
| B.0.1mol·L-1CH3COONa溶液中:c(Na+)=c(CH3COO-)+c(OH-) |
| C.浓度均为0.1mol·L-1的CH3COONa、NaOH和Na2CO3三种溶液的pH大小顺序: pH(NaOH)>pH(Na2CO3)>pH(CH3COONa) |
| D.向0.1mol·L-1CH3COOH溶液中滴加NaOH溶液至中性,溶液中离子浓度的关系: |
c(CH3COO-)>c(Na+)>c(OH-)=c(H+)
下列说法或化学方程式正确的是
A.用坩埚灼烧MgCl2·6H2O的反应式:MgCl2·6H2O MgCl2+6H2O MgCl2+6H2O |
| B.在0.1mol?L-1 Na2SO3溶液中:c(Na+)=2c(SO32―)+ c(HSO3―)+ c(H2SO3) |
| C.常温下,将PH=2的稀硫酸稀释10倍,其中各离子的浓度都变为原来的十分之一 |
| D.蛋白质肽链中-NH-上的氢原子与羰基上的氧原子形成氢键是蛋白质二级结构的主要依据 |
维生素A1、B2的结构简式分别如图所示: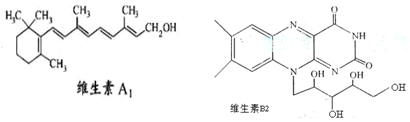
已知: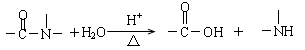
下列说法正确的是
| A.1mol维生素A1最多与溴水中的4molBr2发生加成反应 |
| B.维生素A1的分子式为C19H30O,是一种易溶于水的高分子。 |
| C.维生素B2在酸性条件下彻底水解后得到的有机物,其分子内发生酯化得多种酯 |
| D.用-C4H9取代维生素B2苯环上的一个H原子,最多可得4种同分异构体 |
下列叙述正确的是
A.实验室用右图所示装置制取乙烯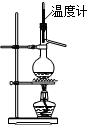 |
| B.由水电离出的c(H+)=10-13mol·L-1的溶液中,Na+、ClO-、K+、I-一定能大量共存 |
| C.肥皂的主要成分是高级脂肪酸盐 |
| D.某温度下Fe(OH)3的KSP=4×10-38,则该温度下, |
饱和溶液的c(OH-)=2×10-19 mol·L-1
短周期元素X、Y、Z三种原子核外电子总数为32,都可形成常温下气体单质。X原子最外层电子数是其内层电子数的3倍;Y的气态氢化物与其最高价氧化物对应的水化物恰好反应的产物只有一种A,A的水溶液显酸性。下列说法正确的是
| A.原子半径: Z>X >Y |
| B.X元素形成的单质其摩尔质量一定是32g·moL-1 |
| C.物质A中既含离子键又含共价键 |
| D.YX2、ZX2都有对应的含氧酸 |
下列说法正确的是
| A.用新制氢氧化铜检验牙膏中的甘油,现象是看到产生蓝色沉淀。 |
| B.少量SO2通入NaClO溶液的离子反应式:SO2+ClO-+H2O=SO42-+Cl-+2H+ |
| C.加热NH4Cl晶体时,在坩埚上方有白烟,其成分是NH4Cl,说明NH4Cl受热升华 |
| D.著名的侯德榜制碱法是饱和食盐水中先后通入足量CO2、NH3析出Na2CO3晶体。 |