下列溶液中的Cl-浓度与50 mL 1 mol·L-1 MgCl2溶液中的Cl-浓度相等的是( )
| A.150 mL 1 mol·L-1 NaCl溶液 | B.75 mL 2 mol·L-1 CaCl2溶液 |
| C.150 mL 2 mol·L-1 KCl溶液 | D.75 mL 1 mol·L-1 AlCl3溶液 |
近年来高铁酸钾(K2FeO4)已经被广泛应用在水处理方面,高铁酸钾的氧化性超过高锰酸钾,是一种集氧化、吸附、凝聚、杀菌的新型高效的多功能水处理剂。高铁酸钾在水处理过程中涉及到的过程正确的有:
①蛋白质的变性 ②蛋白质的盐析 ③胶体的聚沉 ④盐类水解 ⑤焰色反应
⑥氧化还原反应
| A.①②③④ | B.①③④⑥ | C.②③④⑤ | D.②③⑤⑥ |
下列物质的转化在给定条件下能实现的是
①NaAlO2(aq) AlCl3
AlCl3 Al ② NH3
Al ② NH3 NO
NO HNO3
HNO3
③NaCl(饱和) NaHCO3
NaHCO3 Na2CO3 ④FeS2
Na2CO3 ④FeS2 SO3
SO3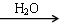 H2SO4
H2SO4
| A.②③ | B.①④ | C.②④ | D.③④ |
下列表示对应化学反应的离子方程式正确的是
| A.工业电解饱和食盐水:2Cl-+ H2O = Cl2↑+ H2↑+ OH- |
B.碳酸钠的水解:CO32-+ 2H2O H2CO3 + 2OH- H2CO3 + 2OH- |
| C.硫酸铝溶液中滴加过量浓氨水:Al3++4 NH3·H2O===AlO+4NH4++2H2O |
| D.用过氧化氢从酸化海带灰浸出液中提取碘:2I-+ H2O2 +2H+ = I2 +2H2O |
设NA为阿伏伽德罗常数的值。下列叙述正确的是
| A.78gNa2O2固体中含有的阴离子数为NA |
| B.标准状况下,2.24L氖气所含原子数为0.2NA |
| C.1L 0.1 mol/L醋酸溶液中含有的氢离子数为0.1NA |
| D.标准状况下,2.24L己烷含有分子的数目为0.1NA |