T℃时,A气体和B气体反应生成C气体。反应过程中A、B、C浓度变化如下图甲所示,若保持其它条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如下图乙所示,则下列结论正确的是
甲 乙
A.t1min时,保持其它条件不变,增大压强,平衡向逆反应方向移动
B.t1min时,保持容器总体积不变,通入少量稀有气体,平衡向逆反应方向移动
C.其它条件不变时,升高温度,正、逆反应速率均增大,且A的转化率减小
D. T℃时,在相同容器中,若有1.0mol/L A、1.4mol/L B开始反应,达到平衡后,C的浓度等于0.8mol/L
下列叙述正确的是
| A.1.00mol NaCl中含有6.02×1023个NaCl分子 |
| B.1.00mol NaCl中,所有Na+的最外层电子总数为8×6.02×1023 |
| C.欲配制1.00L ,1.00mol.L-1的NaCl溶液,可将58.5g NaCl溶于1.00L水中 |
| D.电解58.5g 熔融的NaCl,能产生22.4L氯气(标准状况)、23.0g金属钠 |
根据碘与氢气反应的热化学方程式
(i) I2(g)+ H2(g)  2HI(g)+ 9.48 kJ (ii) I2(S)+ H2(g)
2HI(g)+ 9.48 kJ (ii) I2(S)+ H2(g) 2HI(g) - 26.48 kJ
2HI(g) - 26.48 kJ
下列判断正确的是
| A.254g I2(g)中通入2gH2(g),反应放热9.48 kJ |
| B.1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ |
| C.反应(i)的产物比反应(ii)的产物稳定 |
| D.反应(ii)的反应物总能量比反应(i)的反应物总能量低 |
已知:2Zn(s)+O2(g)=2ZnO(s)△H=-701.0kJ·mol-1
2Hg(l)+O2(g)=2HgO(s)△H=-181.6kJ·mol-1
则反应Zn(s)+ HgO(s)=ZnO(s)+ Hg(l)的△H为
| A.+519.4kJ·mol-1 | B.+259.7 kJ·mol-1 |
| C.-259.7 kJ·mol-1 | D.-519.4kJ·mol-1 |
下列有关化学用语能确定为丙烯的是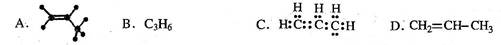
下列固体混合物与过量的稀H2SO4反应,能产生气泡并有沉淀生产的是
| A.NaHCO3和Al(OH)3 | B.BaCl2和NaCl |
| C.HClO3和K2SO4 | D.Na2SO3和BaCO3 |