19世纪中叶,俄国化学家门捷列夫的突出贡献是
| A.提出了原子学说 | B.发现了元素周期律 |
| C.提出了分子学说 | D.发现氧气 |
反应2X(g)+Y(g)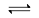 2Z(g);△H<0,在不同温度(T1和T2)下,产物Z的物质的量n与反应时间t的关系如图所示,则下列判断中正确的是()
2Z(g);△H<0,在不同温度(T1和T2)下,产物Z的物质的量n与反应时间t的关系如图所示,则下列判断中正确的是()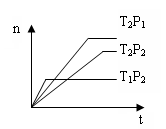
| A.T1<T2,P1<P2 | B.T1<T2,P1>P2 |
| C.T1>T2,P1>P2 | D.T1>T2,P1<P2 |
在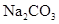 溶液中,下列等量关系成立的是()
溶液中,下列等量关系成立的是()
| A.c(OH-)= c(H+)+c(HCO3-)+2c(H2CO3) |
| B.2c(Na+)= c(CO32-)+ c(HCO3-)+ c(H2CO3) |
| C.c(Na+)+ c(H+)= c(HCO3-) +2c(CO32-)+ c(OH-) |
| D.c(Na+)="2" c(CO32-)+ c(HCO3-)+ c(H2CO3) |
已知 (1)H2(g)+ O2(g)===H2O(g)△H1=a kJ·mol-1
(1)H2(g)+ O2(g)===H2O(g)△H1=a kJ·mol-1
(2)2H2(g)+O2(g)===2H2O(g)△H2=b kJ·mol-1 (3)H2(g)+ O2(g)===H2O(l)△H3=c kJ·mol-1
(3)H2(g)+ O2(g)===H2O(l)△H3=c kJ·mol-1
(4)2H2(g)+O2(g)===2H2O(l)△H4=d kJ·mol-1
下列关系式中正确的是( )
| A.a<c<0 | B.b>d>0 | C.2a=b<0 | D.2c=d>0 |
100℃时,NaCl溶液中c(H+)=1×10-6 mol/L。下列说法中正确的是( )
| A.该NaCl溶液显酸性 |
| B.该NaCl溶液显碱性 |
| C.该NaCl溶液中KW=c(H+)·c(OH-)=1×10-14 |
| D.该NaCl溶液中KW=c(H+)·c(OH-)=1×10-12 |
某化学反应其△H=" —122" kJ·mol-1,∆S="231" J·mol-1·K-1,则此反应在下列哪种情况下,可自发进行:()
| A.在任何温度下都能自发进行 | B.在任何温度下都不能自发进行 |
| C.仅在高温下自发进行 | D.仅在低温下自发进行 |