某化学反应2A(g)  B(g) + D(g)在四种不同条件下进行,反应器均为相同恒容密闭容器,B、D起始浓度为0。反应物A的浓度(
B(g) + D(g)在四种不同条件下进行,反应器均为相同恒容密闭容器,B、D起始浓度为0。反应物A的浓度( )随反应时间(min)的变化情况如下表:
)随反应时间(min)的变化情况如下表:
| 实验 序号 |
|
0 |
10 |
20 |
30 |
40 |
50 |
60 |
| 1 |
800℃ |
1.0 |
0.80 |
0.67 |
0.57 |
0.50 |
0.50 |
0.50 |
| 2 |
800℃ |
C2 |
0.60 |
0.50 |
0.50 |
0.50 |
0.50 |
0.50 |
| 3 |
800℃ |
C3 |
0.92 |
0.75 |
0.63 |
0.60 |
0.60 |
0.60 |
| 4 |
820℃ |
1.0 |
0.40 |
0.25 |
0.20 |
0.20 |
0.20 |
0.20 |
根据上述数据,完成下列填空:
(1)在实验1中,反应在10~20分钟内用A表示的平均速率为 ____________ 。
(2)在实验2中,A的初始浓度C2=  ,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是 。
,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是 。
(3)设实验3的反应速率为υ3,实验1的反应速率为υ1,则υ3 υ1(填>、=、<),且C3=  。
。
(4)由上述实验,可推测该反应是 反应(选填“吸热”或“放热”)。理由是:
。
(5)1~4组实验中,A的平衡转化率最大的是第 组。
(6)在实验2中,50 min后,若将容器体积增大1倍,则达平衡时B的浓度为 _____  ;该反应的平衡常数K (填“不变”或“增大”或“减小”)。
;该反应的平衡常数K (填“不变”或“增大”或“减小”)。
取1.38g K2CO3溶于水配成50ml溶液,求
(1)K2CO3物质的量
(2)K2CO3物质的量浓度
(3)K+、CO32-物质的量浓度
将3 mol A和2.5 mol B混合于2L的密闭容器中,发生反应的化学方程式为:3A(气) + B(气) 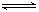 xC(气) + 2D(气),5 min后反应达到平衡状态,容器内的压强变小,已知D的平均反应速度为 0.1 mol/(L﹒min), 填写下列空白:
xC(气) + 2D(气),5 min后反应达到平衡状态,容器内的压强变小,已知D的平均反应速度为 0.1 mol/(L﹒min), 填写下列空白:
(1) x =______
(2) 平衡时C的浓度为 ________________
(3) 平衡时B的转化率为 _____________
(4) 平衡时,容器内的压强与原容器内压强的比值为 ___________
常温下电解200mL一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如下图所示(气体体积已换算成标准状况下的体积),根据图中信息回答下列问题。
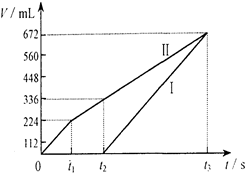
⑴通过计算推测:
①原混合溶液NaCl和CuSO4的物质的量浓度。
②t2时所得溶液的pH。
⑵实验中发现,阳极产生的气体体积与阴极相比,明显小于对应时间段的理论值。试简要分析其可能原因。
在加热条件下,用二氧化锰与足量浓盐酸反应,制得氯气0.56L(标准状况)。问:
(1)理论上需要消耗MnO2多少克?
(2)被氧化的HCl的物质的量是多少?
(3)在反应中,电子转移的数目大约是多少?
实验室使用的浓盐酸的溶质质量分数一般为36.5%,密度为1.19g.cm-3。
(1)求该浓盐酸的物质的量浓度。
(2)将多少升氯化氢(标准状况)通入2.00L水中可得36.5%的浓盐酸?
(3)取一定体积的该盐酸与足量二氧化锰在一定条件下反应,若生成标准状况下氯气33.6L,则被还原的HCl的物质的量是多少?