某学生中和滴定实验的过程如下:
(a)取一支碱式滴定管;
(b)用蒸馏水洗净;
(c)即加入已知浓度的NaOH溶液;
(d)记录液面刻度读数;
(e)用酸式滴定管精确放出一定体积待测酸液;
(f)置于未经待测酸液润洗的洁净锥形瓶中;
(g)加入酚酞试液2滴;
(h)滴定时,边滴边摇荡;
(i)边注视滴定管内液面的变化;
(j)当小心滴到溶液由无色变成粉红色时,即停止滴定;
(k)记录液面刻度读数;
(l)根据滴定管的两次读数得出NaOH溶液体积为22mL。
上述实验过程中的错误之处有:
| A.(c)(f)(i)(j) | B.(c)(f)(i)(j)(l) |
| C.(c)(h)(i)(j) | D.(c)(i)(j)(l) |
如图为某种甲醇燃料电池示意图,工作时电子流方向如图所示。下列判断正确的是
| A.X为氧气 |
| B.电极A反应式:CH3OH-6e-+H2O = CO2+6H+ |
| C.B电极附近溶液pH增大 |
| D.电极材料活泼性:A>B |
下列反应中,同时符合图像Ⅰ和Ⅱ的是
A.N2(g)+3H2(g) 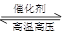 2NH3(g) ΔH<0 2NH3(g) ΔH<0 |
B.2SO3(g)  2SO2(g)+O2(g) ΔH>0 2SO2(g)+O2(g) ΔH>0 |
C.H2(g)+CO(g) 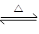 C(s)+H2O(g) ΔH>0 C(s)+H2O(g) ΔH>0 |
D.4NH3(g)+5O2(g) 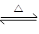 4NO(g)+6H2O(g) ΔH<0 4NO(g)+6H2O(g) ΔH<0 |
下列措施不能增大反应速率的是
| A.锌与稀硫酸反应时,加少量铜粉 |
| B.Fe与稀硫酸反应制取H2时,改用98%浓硫酸 |
| C.Al在氧气中燃烧生成A12O3,将铝片改成铝粉 |
| D.恒温时,增大H2(g)+Br2(g) ⇌2HBr(g)反应体系的压强 |
下列描述不符合生产、生活实际的是
| A.家用炒锅残留盐溶液时易发生吸氧腐蚀 |
| B.电解法精炼粗铜,用纯铜作阴极 |
| C.电解水制氢气时,用铜作阳极 |
| D.在镀件上电镀锌,用锌作阳极 |
已知:N2(g)+3H2(g) ⇌ 2 NH3(g) △H =" -92.4" kJ/mol。一定条件下,现有容积相同且恒容的密闭容器甲与乙:① 向甲中通入1 mol N2和3 mol H2,达到平衡时放出热量Q1 kJ;② 向乙中通入0.5 mol N2和1.5 mol H2,达到平衡时放出热量Q2 kJ。则下列关系式正确的是
| A.92.4>Ql>2Q2 | B.92.4=Q1<2Q2 |
| C.Q1=2Q2=92.4 | D.Q1=2Q2<92.4 |