纳米是长度单位,1纳米等于1×10-9m,物质的颗粒达到纳米级时,具有特殊的性质。例如将单质铜制成“纳米铜”时,具有非常强的化学活性,在空气中可以燃烧。下列对“纳米铜”的有关叙述正确的
| A.常温下“纳米铜”比铜片的金属性强,反应时反应速率快 |
| B.常温下“纳米铜”比铜片更易失电子,反应时反应速率快 |
| C.常温下“纳米铜”与氧气反应的活化能降低了 |
| D.“纳米铜”颗粒更细小,化学反应时接触面大,所以反应速率快。 |
NA表示阿伏加德罗常数,下列说法正确的是
| A.1 mol Na与足量O2反应生成Na2O或Na2O2均失去NA个电子 |
B.1 mol Al分别放入足量的冷的浓HNO3、稀HNO3 中,反应后转移的电子均为3NA个 中,反应后转移的电子均为3NA个 |
| C.各5.6g铁分别与足量的盐酸、氯气反应,电子转移总数均为0.3NA |
| D.2.7g铝与足量的NaOH溶液反应,转移的电子总数为NA |
下列离子方程式正确的是
| A.硫酸与氢氧化钡溶液反应: Ba2++SO42-=BaSO4↓ |
| B.钠与水反应: 2Na+2H2O=2Na++2OH-+H2↑ |
C.向次氯酸钠溶液中通入足量SO2气体: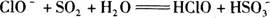 |
| D.Ca(HCO3)2溶液中加入少量NaOH溶液: |
Ca2++2HCO3-+2OH-= CaCO3↓+CO32-+2H2O
已知A、B、C、D均位于前3周期,且 aA2+、bB+、cC3-、dD-核外电子层结构完全相同。则下列有关叙述正确的是
A.原子半径 A>B>D>C B.原子序数d>c>b>a
C.离子半径 C>D>B>A D.单质的还原性 A>B>D>C
Al、Fe、Cu都是重要的金属元素。下列说法正确的是
| A.三者对应的氧化物均为碱性氧化物 |
| B.三者的单质放置在空气中均只生成氧化物 |
| C.制备AlCl3、FeCl3、CuCl2均不能采用将溶液直接蒸干的方法 |
| D.电解AlCl3、FeCl3、CuCl2的混合溶液时阴极上依次析出Cu,Fe,Al |
下列关于化学与生产、生活的认识不正确的是
| A.CO2、CH4、N2等均是造成温室效应的气体 |
| B.使用清洁能源是防止酸雨发生的重要措施之一 |
| C.节能减排符合低碳经济的要求 |
| D.合理开发利用可燃冰(固态甲烷水合物)有助于缓解能源紧缺 |