下列说法中可以证明反应N2+3H2 2NH3已达到平衡状态的是( )
2NH3已达到平衡状态的是( )
| A.1molN≡N键断裂的同时,有3molH-H键生成 |
| B.1molN≡N键断裂的同时,有3molH-H键断裂 |
| C.1molN≡N键断裂的同时,有6molH-H键断裂 |
| D.1molN≡N键断裂的同时,有6molH-H键生成 |
盐酸、醋酸和碳酸氢钠是生活中常见的物质,下列表述正确的是
| A.在NaHCO3溶液中加入与其等物质的量的NaOH,溶液中的阴离子只有CO32-和OH- |
| B.将pH相同的盐酸和醋酸稀释相同倍数,醋酸的pH变化大 |
| C.10 mL0.10 mol·L-1CH3COOH溶液加入等物质的量的NaOH后,溶液中离子的浓度由大到小的顺序是:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| D.中和体积与pH都相同HCl溶液和CH3COOH溶液所消耗NaOH物质的量相同 |
下列各式中属于正确的水解反应的离子方程式的是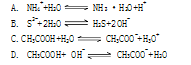
下列说法或表示方法正确的是
| A.等物质的量的硫蒸气和固体硫分别完全燃烧,后者放出热量多 |
| B.由C(石墨)= C(金刚石);△H=+1.90 kJ/mol可知,金刚石比石墨稳定 |
| C.在101kPa时,2g氢气完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)= 2H2O(l) △H=-285.8kJ/mol |
D.在稀溶液中,H+(aq)+ OH-(aq) = H2O(l) △H=-57.3kJ/mol,若将含0.5molH2SO4的浓硫酸与含1molNaOH的溶液混合, 放出的热大于57.3kJ 放出的热大于57.3kJ |
下列说法正确的是
| A.将AlCl3溶液蒸干并灼烧后得到的物质是Al(OH)3 |
| B.向饱和AgCl水溶液中加入盐酸,Ksp值变大 |
| C.温度一定时,当溶液中Ag+和Cl-浓度的乘积等于Ksp值时,此溶液为AgCl的饱和溶液 |
| D.所谓沉淀完全就是用沉淀剂将溶液中某一离子除净; |
已知Ag2SO4的KSP=c2(Ag+)× c(SO42-)=1.4×10-5,将适量Ag2SO4固体溶于100 mL水中至刚好饱和,此时溶液中c(Ag+)=0.030 mol·L-1。若t1时刻改变条件,下图中不正确的是