氢气在氯气中燃烧时产生苍白色火焰。在反应过程中,破坏1mol氢气中的化学键消耗的能量为Q1kJ,破坏1mol氯气中的化学键消耗的能量为Q2kJ,形成1mol氯化氢中的化学键释放的能量为Q3kJ。下列关系式中,正确的是( )
| A.Q1+ Q2>Q3 | B.Q1+ Q2>2Q3 | C.Q1+ Q2<Q3 | D.Q1+ Q2<2Q3 |
下列过程中的化学反应,相应的离子方程式正确的是( )
| A. |
用碳酸钠溶液处理水垢中的硫酸钙: |
| B. |
过量铁粉加入稀硝酸中: |
| C. |
硫酸铝溶液中滴加少量氢氧化钾溶液: |
| D. |
氯化铜溶液中通入硫化氢: |
在实验室采用如图装置制备气体,合理的是( )
|
化学试剂 |
制备气体 |
|
|
A. |
|
|
|
B. |
|
|
|
C. |
|
|
|
D. |
|
|

| A. |
A |
B. |
B |
C. |
C |
D. |
D |
我国提出争取在2030年前实现碳达峰、2060年前实现碳中和,这对于改善环境、实现绿色发展至关重要。"碳中和"是指 的排放总量和减少总量相当。下列措施中能促进碳中和最直接有效的是( )
| A. |
将重质油裂解为轻质油作为燃料 |
| B. |
大规模开采可燃冰作为新能源 |
| C. |
通过清洁煤技术减少煤燃烧污染 |
| D. |
研发催化剂将 还原为甲醇 |
乙醛酸是一种重要的化工中间体,可果用如下图所示的电化学装置合成。图中的双极膜中间层中的 解离为 和 ,并在直流电场作用下分别问两极迁移。下列说法正确的是( )
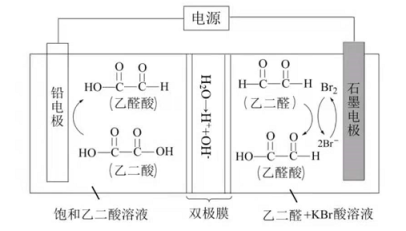
| A. |
在上述电化学合成过程中只起电解质的作用 |
| B. |
阳极上的反应式为: |
| C. |
制得 乙醛酸,理论上外电路中迁移了 电子 |
| D. |
双极膜中间层中的 在外电场作用下向铅电极方向迁移 |
已知相同温度下, 。某温度下,饱和溶液中 、 与 的关系如图所示。

下列说法正确的是( )
| A. |
曲线①代表 的沉淀溶解曲线 |
| B. |
该温度下 的 值为 |
| C. |
加适量 固体可使溶液由a点变到b点 |
| D. |
时两溶液中 |