(10分)近年来,国际原油价格大幅上涨,促使各国政府加大生物能源生产,其中酒精汽油已进入实用化阶段。
(1)乙醇在铜或银作催化剂的条件下,可以被空气中的氧气氧化成X,X可发生银镜反应,请写出X被银氨溶液氧化的反应方程式(标出具体反应条件):
。
(2)乙醇可以与酸性重铬酸钾溶液反应,被直接氧化成Y,Y含有官能团的名称是________。在浓硫酸存在下加热,乙醇与Y反应可生成一种有香味的物质W,化学方程式为 。
(3)现有两瓶无色液体,分别盛有Y、W,只用一种试剂就可以鉴别,该试剂可以是
(4)现代石油化工采用银作催化剂,乙烯能被氧气氧化生成环氧乙烷(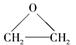 ),该反应的原子利用率为100%,反应的化学方程式为 。
),该反应的原子利用率为100%,反应的化学方程式为 。
在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
| t/℃ |
700 |
800 |
830 |
1 000 |
1 200 |
| K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K= 。
(2)该反应为 反应(填“吸热”或“放热”)。
(3)能判断该反应是否达到化学平衡状态的依据是 。
A.容器中压强不变
B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O)
D.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为 ℃。
高炉炼铁中发生的基本反应之一如下:
FeO(s)+CO(g) Fe(s)+CO2(g) ΔH>0,其平衡常数表达式为K= ,又知1 100 ℃时,K=0.28。
Fe(s)+CO2(g) ΔH>0,其平衡常数表达式为K= ,又知1 100 ℃时,K=0.28。
(1)温度升高,化学平衡移动后达到新的平衡,平衡常数 。(填“变大”“变小”或“不变”)
(2)1 100 ℃时测得高炉中c(CO2)=0.013 mol·L-1,c(CO)=0.05 mol·L-1,在这种情况下,该反应是否处于化学平衡状态: (填“是”或“否”),此时,化学反应速率是v(正) v(逆)(填“大于”“小于”或“等于”),其原因 。
已知H+(aq)+OH-(aq) H2O(l) ΔH=-57.3 kJ·mol-1,回答下列问题。
H2O(l) ΔH=-57.3 kJ·mol-1,回答下列问题。
(1)用含20 g NaOH的稀溶液跟足量稀盐酸反应放出 kJ的热量。
(2)用含2 mol H2SO4的稀溶液跟足量稀NaOH反应,此反应的中和热的ΔH= 。
(3)如果将(1)反应中的稀盐酸换成稀醋酸,反应放出的热量 (填“大于”“小于”或“等于”)原来(1)放出的热量。
下表中的数据是破坏1 mol物质中的化学键所消耗的能量(kJ):
| 物质 |
Cl2 |
Br2 |
I2 |
HCl |
HBr |
HI |
H2 |
| 能量/kJ |
243 |
193 |
151 |
432 |
366 |
298 |
436 |
根据上述数据回答(1)~(5)题。
(1)下列物质本身具有的能量最低的是 。
A.H2 B.Cl2 C.Br2 D.I2
(2)下列氢化物中,最稳定的是 。
A.HCl B.HBr C.HI
(3)X2+H2 2HX(X代表Cl、Br、I )的反应是吸热反应还是放热反应?答: 。
2HX(X代表Cl、Br、I )的反应是吸热反应还是放热反应?答: 。
(4)相同条件下,X2(X代表Cl、Br、I)分别与氢气反应,当消耗等物质的量的氢气时,放出或吸收的热量最多的是 。
(5)若无上表中的数据,你能正确回答出问题(4)吗?
答: ,你的根据是 。
茉莉花香气的成份有多种,乙酸苯甲酯( )是其中的一种,它可以从茉莉花中提取。一种合成路线如下:
)是其中的一种,它可以从茉莉花中提取。一种合成路线如下: 
回答下列问题:
(1)A物质的官能团是,C的结构简式为。
(2)反应③的反应类型为。
(3)写出反应①的化学方程式:。
(4)①②③反应中哪个反应的原子理论利用率为100%,符合绿色化学的要求。
(填序号)