丙酸、甲酸乙酯和乙酸甲酯三种有机物共同具有的性质是 ( )
| A.都能发生加成反应 | B.都能发生水解反应 |
| C.都能跟稀H2SO4反应 | D.都能跟NaOH溶液反应 |
下列各组混合物中,用分液漏斗不能分离的是()
| A.甲苯和水 | B.乙酸乙酯和水 |
| C.丙三醇和水 | D.溴苯和水 |
区别甲烷、乙烯、乙炔最简单的方法是 ( )
| A.分别通入溴水 | B.分别通入酸性KMnO4溶液 |
| C.分别在空气中燃烧 | D.分别通入装有碱石灰的干燥管 |
以石墨电极电解200 mL CuSO4溶液,电解过程中产生气体体积V(g)(标准状况)与电子转移物质的量n(e-)的关系如下图所示,n(e-)=0.8 mol时停止电解。下列说法中正确的是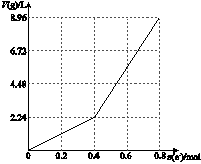
| A.电解前CuSO4溶液的物质的量浓度为2 mol/L |
| B.当n(e-)=0.6 mol时,V(H2)∶V(O2)=2∶3 |
| C.电解后所得溶液中c(H+)=2 mol/L |
| D.向电解后的溶液中加入16 g CuO,则溶液可恢复为电解前的浓度 |
双酚A是食品、饮料包装和奶瓶等塑料制品的添加剂,能导致人体内分泌失调,对儿童的健康危害更大。下列有关双酚A的叙述不正确的是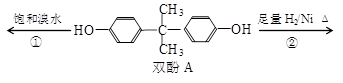
| A.双酚A的分子式是C15H16O2 |
| B.双酚A的核磁共振氢谱显示氢原子数之比是1:2:2:3 |
| C.反应①中,1 mol双酚A最多消耗2 mol Br2 |
| D.反应②的产物中只有一种官能团 |