常温下,某溶液中由水电离产生的c(H+)、c(OH-)满足c(H+)·c(OH-)=10-26,则下列各组离子在该溶液中一定可以大量共存的是
| A.K+、Na+、AlO2-、Cl- | B.Na+、Cl-、SO42-、HCO3- |
| C.NH4+、Fe3+、NO3-、SO42- | D.Ba2+、Na+、Cl-、NO3- |
NA代表阿伏加德罗常数,下列叙述错误的是
| A.10 mL 质量分数为 98 %的 H2SO4,用水稀释至 100 mL , H2SO4的质量分数为 9.8 % | B.在 H2O2 + Cl2 =" 2HCl" + O2反应中,每生成 32g氧气,则转移 2 NA个电子 |
| C.标准状况下,分子数为NA的 CO 、C2H4混合气体体积约为 22 . 4L ,质量为 28g | |
| D.一定温度下, 1 L 0.5 mol/L NH4Cl 溶液与 2 L 0. 25mol/L NH4Cl 溶液含NH4+ 物质的量不同 |
某碱性溶液中只有Na+、CH3COO-、H+、OH-四种离子。则下列描述正确的是( )
| A.pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈蓝色 |
| B.该溶液由等物质的量浓度、等体积的NaOH溶液和CH3COOH溶液混合而成 |
| C.在NaOH溶液中加入一定量的CH3COOH溶液,只有当溶液中离子浓度满足: c(Na+)>c(CH3COO-)>c(OH-)>c(H+)时,才符合题意。 |
| D.加入适量氨水,c(CH3COO-)一定大于c(Na+)、c(NH4+)之和 |
下列有关能量或反应热的说法正确的是()
| A.化石燃料和植物燃料燃烧时放出的能量均来源于太阳能 |
| B.牺牲阳极保护法是电能转化为化学能的过程 |
| C.CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)===2CO(g)+O2(g)反应的△H=+2×283.0kJ/mol |
| D.放热反应一定比吸热反应更容易发生。 |
下列各项叙述中,类比推理正确的是()
| A.铜丝在氧气中燃烧生成是CuO,则铁丝在氧气中燃烧生成Fea2O3 |
| B.少量CO2 通入NaOH溶液中生成Na2CO3 ,则少量CO2 通入C6H5 ONa溶液中也生成Na2CO3 |
| C.甲醛能发生银镜反应,则甲酸甲酯也能发生银镜反应。 |
| D.金刚石的硬度大,则C60的硬度也大。 |
V、W、X、Y、Z是由周期表中1~20号部分元素组成的5种化合物,其中V、W、X、Z均为两种元素组成,上述5种化合物涉及的所有元素的原子序数之和等于35。它们之间的反应关系如下图: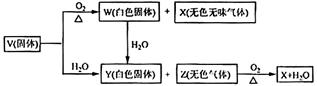
(1)5种化合物分别是V 、W 、X 、Y 、Z :(填化学式)
(2)由上述5种化合物中2种化合物反应可生成一种新化合物,它包含了5种化合物中的所有元素,生成该化合物的化学方程式是 :
(3)V的电子式是 。