同周期的X、Y、Z三元素, 其最高价氧化物水化物的酸性由弱到强的顺序是:H3ZO4<H2YO4<HXO4, 则下列判断正确的是( )
| A.原子半径 X>Y>Z |
| B.非金属性 X>Y>Z |
| C.阴离子的还原性按X、Y、Z的顺序由强到弱 |
| D.气态氢化物的稳定性按X、Y、Z的顺序由弱到强 |
下列反应中,氧化剂与还原剂物质的量之比为1∶2的是
| A.3S+6NaOH===2Na2S+Na2SO3+3H2O |
| B.2CH3COOH+Ca(ClO)2===2HClO+Ca(CH3COO)2 |
| C.I2+2NaClO3===2NaIO3+Cl2 |
D.4HCl(浓)+MnO2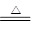 MnCl2+Cl2↑+2H2O MnCl2+Cl2↑+2H2O |
根据表中信息,判断下列叙述中正确的是
| 序号 |
氧化剂 |
还原剂 |
其他反应物 |
氧化产物 |
还原产物 |
| ① |
Cl2 |
FeBr2 |
/ |
Fe3+、Br2 |
|
| ② |
KClO3 |
浓盐酸 |
/ |
Cl2 |
|
| ③ |
KMnO4 |
H2O2 |
H2SO4 |
O2 |
Mn2+ |
A.由表中①组的信息可知通入Cl2的量不同,氧化产物可能不同
B.反应①中,当只有少量Cl2时,反应可表示为Cl2+ Fe2+===Fe3++ 2Cl-
C.表中②组反应的还原产物是KCl,电子转移数目是6e-
D.表中③组反应的离子方程式为2MnO+ 3H2O2+6H+===2Mn2++ 4O2↑+ 6H2O
由于做实验时不小心使皮肤粘上了一些高锰酸钾粉末,形成的黑斑很久才能消除。如果用草酸(乙二酸)的稀溶液洗涤,黑斑可以迅速褪去,其离子方程式为: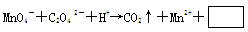
则下列有关叙述正确的是
| A.发生还原反应的是C2O4 2― |
| B.该离子方程式右侧方框内的产物是OH― |
| C.10mol H+ 参加反应时,电子转移5mol |
| D.1mol草酸分子中含有9mol共用电子对 |
某一反应体系中有反应物和生成物共6种:HCl、H2SO4、SnCl2、SnCl4、FeSO4、Fe2(SO4)3,已知反应前在溶液中滴加KSCN溶液呈血红色,反应后红色消失。则该反应中的氧化剂和氧化产物分别是
| A.SnCl4、Fe2(SO4)3 | B.Fe2(SO4)3、SnCl4 |
| C.SnCl2、FeSO4 | D.HCl、H2SO4 |
下列叙述正确的是
| A.发生化学反应时失去电子越多的金属原子,还原性越强 |
| B.金属阳离子被还原后,一定得到该元素的单质 |
| C.核外电子总数相同的原子,一定是同种元素的原子 |
| D.化合反应和置换反应均属于氧化还原反应 |