.某同学对“NaOH和NH4Cl都是离子化合物”,有下列四点感悟,其中不正确的是
| A.离子化合物中可能含共价键 | B.离子化合物中一定含离子键 |
| C.离子化合物中不一定含金属元素 | D.离子化合物中一定含共价键 |
已知H—H键能为436 kJ·mol-1,H—N键能为391 kJ·mol-1,根据化学方程式:
N2+3H2 2NH3ΔH=-92.4 kJ·mol-1,则N≡N键的键能是
2NH3ΔH=-92.4 kJ·mol-1,则N≡N键的键能是
| A.431 kJ·mol-1 | B.946 kJ·mol-1 | C.649 kJ·mol-1 | D.869 kJ·mol-1 |
下列说法不正确的是
| A.外界条件相同时,放热反应的速率一定大于吸热反应的速率 |
| B.化学反应中的能量变化可表现为热量的变化 |
| C.反应物的总能量高于生成物的总能量时,发生放热反应 |
| D.CaO+H2O=Ca(OH)2反应过程中,旧键断裂吸收的能量小于新键形成释放的能量 |
最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程。反应过程的示意图如下,关于下列说法正确的是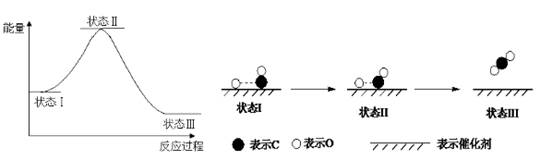
| A.CO和O生成CO2是吸热反应 |
| B.在该过程中,CO断键形成C和O |
| C.CO和O生成了具有极性共价键的CO2 |
| D.状态Ⅰ→状态Ⅲ表示CO与O2反应的过程 |
化学与生产、生活密切相关。下列叙述中,不正确的是
| A.在现实生活中,电化学腐蚀要比化学腐蚀严重的多,危害更大 |
| B.用活性炭为糖浆脱色和用臭氧漂白纸浆,原理不同 |
| C.钢铁制品和铜制品既能发生吸氧腐蚀又能发生析氢腐蚀 |
| D.在铜的精炼装置中,通常用粗铜作作阳极,精铜作阴极 |
亚氯酸钠是一种高效氧化型漂白剂,主要用于棉纺、亚麻、纸浆等漂白。亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都具有漂白作用,但ClO2是毒性很大的气体。经测定,25℃时各组分含量随pH变化情况如图所示(Cl-没有画出)。在25℃时,下列分析正确的是
| A.使用该漂白剂的最佳pH为3 |
B.pH=5时,溶液中 |
| C.pH=7时,溶液中含氯微粒的浓度大小为: c(HClO2)>c( ClO2- )> c( ClO2) >c( Cl-) |
| D.NaClO2溶液加水稀释所有离子浓度均减小 |