一定条件下反应2AB(g) 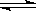 A2(g)+B2(g) 达到平衡状态的标志是
A2(g)+B2(g) 达到平衡状态的标志是
A.单位时间内生成nmolA2,同时消耗2n molAB
B.容器内,三种气体AB、A2、B2共存
C.AB的消耗速率等于A2的消耗速率
D.容器中各组分的体积分数不随时间变化
NO和CO都是汽车排放尾气中的有害物质,它们能缓慢地反应,生成N2和CO2,对此反应下列叙述正确的
| A.使用催化剂并不能改变反应速率 | B.使用催化剂可以加快反应速率 |
| C.降低压强能加快反应速率 | D.降温可以加快反应速率 |
决定化学反应速率的根本因素是
| A.温度和压强 | B.反应物的浓度 | C.参加反应的各物质的性 质 质 |
D.催化剂的加入 |
在气体反应中,能使反应物中活化分子数和活化分子百分数同时增大的方法是
①增大反应物的浓度②升高温度③增大压强④移去生成物⑤加入催化剂
A.②⑤ B.①②③⑤ C.①②③ D .①②③④⑤
.①②③④⑤
25℃、101 kPa下,碳、氢气、甲烷和葡萄糖的燃烧热依次是393.5 kJ/mol、285.8 kJ/mol、890.3 kJ/mol、2800 kJ/mol,则下列热化学方程式正确的是
| A.C(s)+ O2(g)=CO(g);△H=-393.5 kJ/mol |
| B.2H2(g)+O2(g)=2H2O(g);△H=+571.6 kJ/mol |
| C.CH4(g)+2O2(g)=CO2(g)+2H2O(g);△H=-890.3 kJ/mol |
| D.1/2C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l);△H=-1400 kJ/mol |
Cu2S与一定浓度的HNO3反应,生成Cu(NO3)2、CuSO4、NO2、NO和H2O,当N O2和NO的物质的量为1∶1时,实际参加反应的Cu2S与HNO3的物质的量之比为
O2和NO的物质的量为1∶1时,实际参加反应的Cu2S与HNO3的物质的量之比为
| A.1∶7 | B.1∶9 | C.1∶5 | D.2∶9 |