下列有关化学用语正确的是
A.溴化钠的电子式: |
B.氮气分子的结构式:N ≡N |
C.硫原子的结构示意图: |
D.氯化氢分子的电子式: H+[ ]- ]- |
已知 C2H2(g)+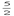 O2=2CO2(g)+H2O(l) △H=-1300kJ/mol 下列说法正确的是 (NA为阿伏加德罗常数值 )
O2=2CO2(g)+H2O(l) △H=-1300kJ/mol 下列说法正确的是 (NA为阿伏加德罗常数值 )
| A.有10NA个电子转移时,该反应吸收1300kJ的能量 |
| B.有NA个水分子生成且为气体时,放出1300kJ的能量 |
| C.有22.4升乙炔气体参与反应时,放出1300kJ的能量 |
| D.有8NA个碳氧共用电子对生成时,放出1300kJ的能量 |
在烃分子中去掉2个氢原子形成一个双键是吸热反应,大约需117kJ/mol~125kJ/mol的热量,但1,3—环己二烯失去2个氢原子变成苯是放热反应,△H=-23.4kJ/mol,以上事实表明
| A.1,3—环己二烯加氢是吸热反应 | B.苯加氢生成环己烷是吸热反应 |
| C.1,3—环己二烯比苯稳定 | D.苯比1,3—环己二烯稳定 |
X、Y二元素的原子,当它们分别获得两个电子形成稀有气体元素原子的电子层结构时,X放出的热量大于Y放出的热量;Z、W两元素的原子,当它们分别失去一个电子形成稀有气体元素原子的电子层结构时,吸收能量W大于Z。则X、Y和Z、W分别形成的化合物中,离子化合物可能性最大的是
| A.Z2X | B.Z2Y | C.W2X | D.W2Y |
氢气(H2)、一氧化碳(CO)、辛烷(C8H18)、甲烷(CH4)的热化学方程式分别为:
H2(g)+1/2O2(g)=H2O(l) △H=-285.8 kJ/mol
CO(g)+1/2O2(g)=CO2(g) △H=-283.0 kJ/mol
C8H18(l)+25/2O2(g)= 8CO2(g)+9H2O(l) △H=-5518 kJ/mol
CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890.3 kJ/mol
相同质量的H2、CO、C8H18、CH4完全燃烧时,放出热量最少的是
| A.H2(g) | B.CO(g) | C.C8H18(l) | D.CH4(g) |
.将0.2mol某烷烃完全燃烧后,生成的气体缓缓通过0.5L 2mol/L的NaOH溶液中,生成正盐和酸式盐的物质的量之比为1:3,则该烷烃是
| A.甲烷 | B.乙烷 | C.丙烷 | D.丁烷 |