在密闭容器中进行如下反应:H2(g) +I2(g) 2HI(g),在温度T1和T2时,产物的量与反应时间的关系如下图所示.符合图示的正确判断是
2HI(g),在温度T1和T2时,产物的量与反应时间的关系如下图所示.符合图示的正确判断是
| A.T1>T2,ΔH>0 |
| B.T1>T2,ΔH<0 |
| C.T1<T2,ΔH>0 |
| D.T1<T2,ΔH<0 |
在容积相同的甲、乙两个密闭容器中,均分别加入3molSO2和1mol O2,同时发生下列反应: 2SO2(g) + O2(g)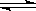 2SO3(g),在相同温度下达到平衡。若甲容器保持体积不变,乙容器保持压强不变,测得甲容器中SO2的转化率为10%,则下列说法中正确的是()
2SO3(g),在相同温度下达到平衡。若甲容器保持体积不变,乙容器保持压强不变,测得甲容器中SO2的转化率为10%,则下列说法中正确的是()
| A.反应过程中的某时刻,甲容器中的反应速率比乙中的大 |
| B.达到平衡时,甲容器反应所需时间比乙容器少 |
| C.乙容器中SO2的转化率大于10% |
| D.平衡时,乙容器中SO2、O2、SO3的浓度之比一定为2:1:2 |
可逆反应H2(g)+I2(g)  2HI(g)
2HI(g) H<0, 达到平衡后,当改变外界条件如物质浓度、体系压强等而发生下列项目的变化时,能做为平衡一定发生了移动的标志的是()
H<0, 达到平衡后,当改变外界条件如物质浓度、体系压强等而发生下列项目的变化时,能做为平衡一定发生了移动的标志的是()
| A.气体的密度变小了 | B.反应物和生成物浓度均变为原来的2倍 |
| C.气体的颜色变深了 | D.体系的温度发生了变化 |
下列反应中,熵显著减少的反应是 ()
| A.CO(g)+2H2(g)= CH3OH(g) |
| B.CaCO3(s)+2HCl(aq)= CaCl2(aq)+CO2(g)+H2O(l) |
| C.(NH4)2CO3(s)= NH4HCO3(s)+NH3(g) |
| D.2HgO(s)= 2Hg(l)+O2(g) |
pH=1的两种一元酸HX和HY溶液,分别取100mL加入足量的镁粉,充分反应后,收集到H2体积分别为VHX和VHY。若相同条件下VHX>VHY,则下列说法正确的 ()
| A.HX可能是强酸 | B.HY一定是强酸 |
| C.HX的酸性强于HY的酸性 | D.反应开始时二者生成H2的速率相等 |
在下图各烧杯中盛有海水,铁在其中腐蚀速率由快到慢的顺序是()。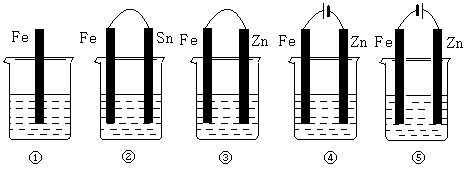
| A.①>②>③>④>⑤ | B.⑤>④>③>②>① |
| C.④>②>①>③>⑤ | D.②>③>⑤>①>④ |