100℃时向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH=2,下列叙述不正确的是
| A.此时水的离子积KW=1.0×10-14 | B.水电离出的c(H+)=1.0×10-10mol/L |
| C.水的电离度随温度升高而升高 | D.c(H3O+)>c(SO42-) |
下列各组物质中,化学键类型和化合物类型都相同的是
| A.SO2和H2O | B.CO2和Na2CO3 |
| C.KOH和NaCl | D.NaCl和HCl |
下列分子中所有原子都满足最外层8电子稳定结构的是
| A.六氟化氙(XeF6) | B.次氯酸(HClO) |
| C.二氧化碳(CO2) | D.三氟化硼(BF3) |
下列各项中表达正确的是
A.H、D、T表示同一种核素
B.F-离子结构示意图
C.用电子式表示HCl形成过程
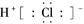
D.次氯酸电子式
关于元素周期表和元素周期律的应用有如下叙述:
①元素周期表是同学们学习化学知识的一种重要工具;
②利用元素周期表可以预测新元素的原子结构和性质;
③利用元素周期表和元素周期律可以预言新元素;
④利用元素周期表可以指导寻找某些特殊的材料。
其中正确的是
| A.①②③④ | B.②③④ |
| C.③④ | D.②③ |
原子核外电子是有规律地进行排布的,它们分层排布在K、L、M、N、O……层上,下列叙述正确的是
| A.K层上容纳的电子数只能是2个 |
| B.K层上容纳的电子数可以超过2个 |
| C.L层上最多只能容纳8个电子 |
| D.最外层上容纳的电子数可以超过8个 |