下列说法或表示法正确的是( )
| A.在化学反应过程中,发生物质变化的同时不一定发生能量变化 |
| B.在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,则表示氢气燃烧热的热化学方程式为2H2(g)+O2(g)===2H2O(l) ΔH=-571.6 kJ/mol |
| C.温度、浓度的改变一定会引起反应速率的改变,所以化学平衡一定会移动 |
| D.酸与碱恰好完全反应生成正盐的c(H+)=c(OH-)=10-6 mol/L的溶液一定呈中性 |
某密闭容器中充入等物质的量的气体A和B,一定温度下发生反应是:
A(g)+xB(g) 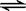 2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的如下图所示。下列说法中正确是
2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的如下图所示。下列说法中正确是

| A.8min前正反应速率大于逆反应速率 |
| B.20min时A的反应速率为0.05mol/(L·min) |
| C.反应方程式中的x=1,正反应为吸热反应 |
| D.30min时降低温度,40min时升高温度 |
已知:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。如图所示,将少量试剂分别放入培养皿中的相应位置,实验时将浓盐酸滴在KClO3晶体上,并用表面皿盖好。下表中由实验现象得出的结论完全正 确的是( )
确的是( )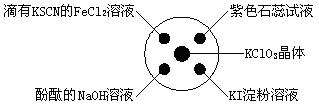
| 选项 |
实验现象 |
结论 |
| A |
滴有KSCN的FeCl2溶液变红色 |
Cl2具有还原性 |
| B |
滴有酚酞的NaOH溶液褪色 |
Cl2具有酸性 |
| C |
石蕊溶液先变为红色后褪色 |
Cl2具有漂白性 |
| D |
KI淀粉溶液中变蓝色 |
Cl2具有氧化性 |
下列叙述中完全正确的一组是()
①常温常压下,1 mol甲基(—CH3)所含的电子数为10NA
②由Cu、Zn和稀硫酸组成的原电池中,若Cu极生成0. 2 g H2,则电路通过电子0.2NA
③在标准状况下,11.2 L NO与11.2 L O2混合后气体分子数为0.75NA
④常温常压下,16 g O3所含的原子数为NA
⑤1 mol C10H22分子中共价键总数为31NA
⑥1 mol Cl2发生反应时,转移的电子数一定是2NA
⑦标准状况下22. 4 L水中含分子数为NA
| A.①②③④⑤ | B.②④⑤⑥⑦ | C.②④⑤ | D.①②⑤ |
下列各组解释合理的是()
| 物质的检验、制备和用途及实验现象 |
解释 |
|
| A |
在一定浓度的乙酸溶液中加入少量乙酸钠固体,溶液pH增大 |
完全是由于乙酸根水解所致 |
| B |
向少量未知溶液中滴加氯化钡溶液,有白色沉淀生成 |
该溶液中一定含有SO2-4 |
| C |
常温下可用铁或铝制容器来盛装浓硫酸或浓硝酸 |
铁、铝表面发生了钝化现象 |
| D |
向饱和NaCl溶液中通入足量的NH3和CO2,有NaHCO3固体析出 |
NaHCO3是难溶于水的盐 |
某物质的晶体内部一个截面上原子的排布情况如右图
|
所示,则该晶体的化学式可表示为
