某食用白醋是由醋酸与纯水配制而成,用中和滴定的方法准确测定其中醋酸的物质的量浓度。实验步骤:①配制500mL浓度约为0.1 mol·L-1的NaOH溶液;②用物质X的标准溶液准确测定该NaOH溶液的浓度(X与氢氧化钠按物质的量比1:1完全反应);③用已知准确浓度的NaOH溶液测定醋酸的浓度。
(1)称量所需的NaOH固体置于大烧杯中,加入500mL蒸馏水,搅拌溶解。该配制步骤__________(填“可行”或“不可行”)。
(2)称量时NaOH在空气中极易吸水,配制所得的NaOH溶液浓度通常比预期_____(填“小”或“大”),这是不能直接配制其标准溶液的原因。
(3)查阅白醋包装说明,醋酸含量约为6g/100mL,换算成物质的量浓度约为_____ mol·L-1,滴定前将白醋稀释_________(填“10”或“100”)倍。(已知醋酸的相对分子质量为60)
(4)稀释白醋时需要的仪器有烧杯、玻璃棒、滴管、酸式滴定管、___________。
(5)准确量取稀释后的白醋20.00mL,置于250mL锥形瓶中,加水30mL,再滴加酚酞指示剂,用上述NaOH标准溶液滴定至____________即为终点。重复滴定两次,平均消耗NaOH标准溶液V mL(NaOH溶液浓度为c mol·L-1)。
(6)原白醋中醋酸的物质的量浓度=____________ mol·L-1。
A、B、C均为短周期元素,在元素周期表中的相对位置如下图所示,A、C两种元素的原子核外电子数之和等于B原子的核电荷数。请完成下列填空: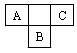
(1)A的原子结构示意图为,A的最高价氧化物对应水化物的的分子式为。
(2)B的简单离子的电子式为。
(3)用电子式表示C的氢化物分子的形成过程: 。
。
(4)C单质与水反应的化学方程式为。
下表列出了A~R等9种元素在元素周期表中的位置:
| 族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
| 2 |
E |
F |
||||||
| 3 |
A |
C |
D |
G |
R |
|||
| 4 |
B |
H |
请按要求用相应的化学用语回答下列问题:
(1)写出下列元素的元素符号:A;E;G。
(2)上述9种元素中,性质最不活泼的元素的一种同位素的原子核内有20个中子,则表示该同位素原子的符号为。
(3)A、C、 D三种元素按金属性由强到弱的顺序排列为。
D三种元素按金属性由强到弱的顺序排列为。
(4)F单质的电子式为。
(5)D元素的最高价氧化物对应的水化物与KOH溶液反应的离子方程式为
。
关于元素周期表的第三周期元素,请用相应的元素符号或化学式回答:
(1)除稀有气体外,原子半径最大的元素是。
(2)非金属性最强的元素是;金属性最强的元素的。
(3)最高价氧化物对应的水化物中,呈两性的物质的化学式为。
(4)最高价氧化物对应的水化物中,碱性最强的物质的化学式为。
(8分) SiC又叫金刚砂,是砂轮的主要成分,可看着是金刚石里一半碳原子被硅原子替换的产物。
①工业上用焦炭和石英在高温下反应制得SiC:3C+SiO2 SiC+2CO。在该反应中氧化剂和还原剂的物质的量比为。
SiC+2CO。在该反应中氧化剂和还原剂的物质的量比为。
②SiC晶体中有两个含五个原子的基本结构单元,分别是和。
③SiC晶体中最小的原子环是圆环,该环独立有个Si原子,个C原子。
④1molSiC晶体中含mol Si-C键。
⑤金刚石、SiC晶体、晶体Si 熔点由高到低的顺序。
已知NiXO晶体晶胞结构为NaCl型(见19题图),由于晶体缺陷,x值于小于1。测知NiXO晶体密度ρ
 为5. 71g·cm-3,晶胞边长为4.28×10-10m(Ni的相对原子质量为58.7,O的相对原子质量为16)。求:(已知:4.283="78.4"
为5. 71g·cm-3,晶胞边长为4.28×10-10m(Ni的相对原子质量为58.7,O的相对原子质量为16)。求:(已知:4.283="78.4" 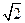 =1.4)
=1.4)
(1)晶胞中两个Ni原子之间的最短距离___________(精确至0.01)。
(2)与O2-距离最近且等距离的Ni离子围成的几何体形状_______
(3)求NiXO中x值为_________(精确至0.01)。
(4)晶体中的Ni分别为Ni2﹢、Ni3﹢,求此晶体的化学式_________。