A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A元素的离子不含电子;B元素的最高价氧化物对应水化物与其氢化物能反应生成盐F;D与A同主族,且与E同周期;E元素原子的最外层电子数是其次外层电子数的3/4,A、B、D、E这四种元素,每一种与C元素都能形成元素的原子个数比不相同的若干种化合物。请回答下列问题:
(1)E元素在元素周期表中的位置是
(2)由A、B、C三种元素形成的离子晶体的化学式为 。
(3)A、C、E间可形成甲、乙两种三原子分子,且甲有18个电子、乙有10个电子,甲与乙比较,沸点较高的是(填化学式) ,用符号和分子的结构式表示出沸点较高的原因为(至少写出两分子) 。
(4)F含有的化学键类型是 ,其水溶液呈酸性,请用相关的离子方程式解释其原因
。
(5)D和C形成的一种化合物能与A和C形成的一种化合物反应产生C单质,该过程的化学方程式为 。
GaAs是仅次于硅的一种新型化合物半导体材料,其性能比硅更优越。Ga位于周期表的第ⅢA族,As位于周期表的第ⅤA族。
(1)Ga和As的最外层电子数分别是_____________________________________________。
(2)GaAs中Ga和As的化合价分别是___________________________________________。
(3)第ⅣA族的C和Si也可以形成类似的化合物半导体材料,该化合物半导体材料的化学式可表示为__________________。
下图表示NH4NO3和D物质为初始反应物发生的一系列变化,其中,在常温下B为液态,F为不溶于水但可溶于酸的白色固体,G与I为无色气体,G能使湿润的红色石蕊试纸变蓝。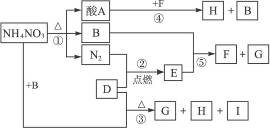
(1)D和H的化学式:D_____________,H_____________,G与E的电子式:G_____________, E_____________。
(2)写出下列反应的方程式:反应①_____________;反应②_____________。
氮可以形成多种离子,如N3-、 、
、 、
、 、
、 、
、 等,已知
等,已知 与
与 是由中性分子结合质子形成的,有类似于
是由中性分子结合质子形成的,有类似于 的性质,另外氮与氢也能形成NH3、N2H4、N3H5、N4H6、N5H7……
的性质,另外氮与氢也能形成NH3、N2H4、N3H5、N4H6、N5H7……
(1)一个 含有__________________________个电子,
含有__________________________个电子, 的电子式为____________。
的电子式为____________。
(2)形成 的中性分子的结构式是_____________________。
的中性分子的结构式是_____________________。
(3) 在强碱溶液中反应的离子方程式:_____________________________。
在强碱溶液中反应的离子方程式:_____________________________。
(4)NH3、N2H4、N3H5、N4H6、N5H7是否互为同系物,为什么?__________________________。
(5)写出N5H7可能的结构简式______________________________。
(6)这一系列化合物中N的质量分数最大值应小于____________%。
在一定条件下,某元素的氢化物X可完全分解为两种单质Y和Z。若已知:
①反应前的X与反应后生成的Z的物质的量之比n(X)∶n(Z)=2∶3。
②单质Y的分子为正四面体构型。
请填写下列空白。
(1)单质Y是______________,单质Z是_________________(填写名称或化学式)。
(2)Y分子中共含________________个共价键。
(3)X分解为Y和Z的化学方程式为:____________________________________。
下图是A→E五种含氮物质的相互转化关系图。其中A、B、C、D常温下都是气体,B为红棕色,写出A、B、C、D、E的化学式和各步反应的化学方程式。
(1)各物质的化学式:
A.____________,B.____________,C.____________,D.____________,E.____________。
(2)各步反应的方程式为:
①____________________________________________________________________________。
②____________________________________________________________________________。
③____________________________________________________________________________。
④____________________________________________________________________________。